Jules Pflanzenblog
Sonntag, 28. Februar 2016
Die Zelle: Aufbau und Aufgaben
Die pflanzliche Zelle, ihr Aufbau, die Bestandteile und deren Aufgaben ist ein hochkomplexes Themengebiet und meiner Meinung nach eher kompliziert. Ich habe deshalb versucht das Thema möglichst kurz zu fassen und übersichtlich zu gliedern.
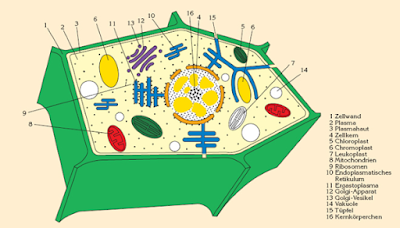
Zellaufbau und Aufgaben
- Zellwand
- Vakuolen
- Protoplasma
- totes Gewebe, mehrschichtig, besteht aus Cellulose
- ist komplett durchlässig (Wasser UND Nährstoffe)
- enthält Tüpfel (Kanäle), diese sind mit Plasmafäden durchzogen (Austausch zwischen Nachbarzellen)
- enthält Intermizellarräume (Hohlräume zwischen den verschiedenen Zellwandschichten)
- sind Hohlräume in der Zelle
- speichern Reservestoffe, Farbstoffe, Abfallprodukte, etherische Öle und Alkaloide
- enthalten Zellsaft
- besteht aus 80% Wasser und Eiweißen
- darin sind alle Zellbestandteile eingebettet
- ist semipermeabel (halbdurchlässig), lässt nur Wasser durch
- grenzt nach innen gegen Vakuolen ab, nach außen gegen die Zellwand ab
- Träger der Erbanlagen
- steuert alle Stoffwechselvorgänge der Zelle
- enthält Kernkörperchen (bilden Ribosome)
- Chloroplasten --> enthalten Chlorophyll
- Chromoplasten --> enthalten Farbstoffe Carotin & Xanthophyll
- Leukoplasten --> speichern Reservestoffe, dazu wandeln sie Traubenzucker in Stärke um
- in ihnen erfolgt die Atmung
- "Kraftwerke" der Zelle, Energie wird bei Atmung freigesetzt
- baut ATP auf
- produzieren Proteine (Eiweiße)
- sind frei in der Zelle, oder am endoplasmatischen Retikulum
- System feinster Röhrchen
- verbindet Zellkern mit Zellwand
- ist durch Plasmafäden mit endoplasm. Retikeln der Nachbarzellen verbunden
- dient der Reizübertragung
- mit Ribosomen besetzt betreibt das e.R. Eiweißsynthese
- bildet Drüsensekrete
- dient der Zellwandneubildung
- sortiert/ verteilt Proteine
- Golgi-Vesikel = abgeschnürte Teile
- Golgi-Vesikel transportieren Schadstoffe aus dem Plasma hinaus
Mittwoch, 17. Februar 2016
Die Zwischenprüfung..oder: Kaffee intravenös, bitte!
Wie auch immer das heute läuft. unsere Ausbildungsgruppe wird danach gepflegt einen trinken gehen, sich selbst feiernd, wissend das die Hälfte überstanden ist und der Kopf noch dran ist.
Drückt uns die Daumen und wünscht uns Erfolg, denn GLÜCK muss man nur Leuten wünschen, die nix drauf haben. Erstmal Kaffee trinken, ein Grundnahrungsmittel für alle Prüflinge..
Kaffee intravenös

Track listing


Rate/Catalog
20 Issues
mixing , performer , producer A1-A3, A5-A6, B1-B5 , remixer A4
mixing
engineer
photography , cover art
116 Reviews
Vote down content which breaks the rules.



Track listing
mixing , performer , producer A1-A3, A5-A6, B1-B5 , remixer A4
mixing
engineer
photography , cover art
Comments
the harvest years with jam to lace the bread
So goodness, goodness knows why I'd throw it to the birds"
Discussion
Contributions
Advertisers are not allowed to run annoying ads on RYM. You can use this form to report problematic or annoying ads.
If you are still on the page where the annoying ad was (or still is) displayed, then proceed to fill out this form.
If the ads navigated you to another page, then use the back button to navigate back to the exact page where the problem started and submit from there.
What is problematic about the ad?
The ad is playing sound without having interacted with it. The ad partially covered site content The ad completely covered site content (like a popup, but without opening a new window) The ad opened a new tab or window The ad redirected my mobile browser to the app store or another app Other (please clarify in comments)
Which ad on the page is the source of the problem? (if there are multiple, just pick the worst one)
Guarana: Anwendungen, Nebenwirkungen, Wechselwirkungen und Warnungen
Brazilian Kakao, Kakao BRASILIEN, Guarana Seed Extract, Guaranine, Paullinia cupana, Paullinia sorbilis, Zoom.
Guarana ist eine Pflanze für die Guarani Stamm im Amazonas benannt, der die Samen verwendet, um ein Getränk zu brauen. Heute, Guarana Samen werden immer noch als Medizin verwendet; Guarana ist zur Gewichtsreduktion eingesetzt, zur Verbesserung der sportlichen Leistung, als Stimulans und geistige und körperliche Ermüdung zu reduzieren. Es ist eine häufige Zugabe zu Energie und Gewichtsverlust Produkte; Einige Leute auch Guarana verwenden, um einen niedrigen Blutdruck und chronischem Erschöpfungssyndrom (CFS) zu behandeln, und Malaria und Ruhr zu verhindern. Es wird auch zur Verbesserung der sexuellen Lust, zu erhöhen, den Harnfluss und als Adstringens verwendet wird; Andere Anwendungen umfassen die Behandlung von chronischer Durchfall, Fieber, Herzprobleme, Kopfschmerzen, Gelenkschmerzen, Rückenschmerzen, und Hitzestress; In der Lebensmittelherstellung, Guarana wurde als Aromastoff in Getränken und Süßigkeiten verwendet.
Guarana enthält Koffein. Koffein wirkt, indem es das zentrale Nervensystem zu stimulieren (ZNS), Herz und Muskeln. Guarana enthält auch Theophyllin und Theobromin, die Chemikalien ähnlich wie Koffein sind.
Zu wenig Beweise fo; Angst. Frühe Forschung deutet darauf hin, dass die Einnahme von zwei Tabletten eines bestimmten Produkts (Euphytose) enthält, Weißdorn, schwarze horehound, Passionsblume, Baldrian, Kolanuss und Guarana dreimal täglich für 28 Tage Angst bei manchen Menschen zu reduzieren. Es ist jedoch nicht klar, ob Guarana allein von Vorteil ist; Mental Leistung. Frühe Forschung bei gesunden Menschen legt nahe, dass eine Einzeldosis von Guarana-Trockenextrakt nehmen Denken Geschwindigkeit verbessern kann. Aber auch andere Untersuchungen zeigen, dass Guarana Einnahme täglich nicht psychische Funktion bei Erwachsenen oder älteren Menschen nicht verbessert; Gewichtsverlust. Guarana könnte Gewichtsverlust zu fördern, wenn sie in Kombination mit Mate und Damiana verwendet. Es gibt auch die Entwicklung Beweise dafür, dass eine bestimmte Kombination Produkt mit Guarana, Ephedra, und 17 andere Vitamine, Mineralien und Nahrungsergänzungsmittel (Metabo-356) helfen, Gewicht von etwa 2,7 kg über acht Wochen, in denen mit einer fettarmen Diät und Bewegung verwendet verringern könnte . Jedoch ist mehr Beweise erforderlich Guarana für diesen Einsatz zu bewerten; Malaria; Durchfall; Fieber; Kopfschmerzen; Herzprobleme; Die Verbesserung der Belastungs Ausdauer; Verbesserung der kurzfristigen, mit hoher Intensität Leistung und Macht; Eine Erhöhung der Blutdruck bei Menschen, die einen niedrigen Blutdruck haben; Chronisches Erschöpfungssyndrom (CFS); Gelenkschmerzen; Flüssigkeitsretention; Andere Bedingungen. Weitere Beweise benötigt Guarana für diese Anwendungen zu bewerten.
Guarana ist wahrscheinlich, sicher für die meisten Erwachsenen, wenn sie in Mengen gefunden häufig in Lebensmitteln verzehrt; Guarana ist wahrscheinlich sicher, wenn mein Mund in der medizinischen Mengen für kurze Zeit eingenommen werden; Guarana ist volle Aufmerksamkeit, wenn durch den Mund in hohen Dosen für eine lange Zeit. Dosen von mehr als 250 bis 300 mg täglich in Verbindung gebracht wurden zu Nebenwirkungen. Nebenwirkungen sind abhängig von der Dosis. Bei typischen Dosen kann das Koffein in Guarana verursachen Schlaflosigkeit, Nervosität und Unruhe, Magenreizungen, Übelkeit, Erbrechen, erhöhte Herzfrequenz und Blutdruck, schnelle Atmung, Zittern, Delirium, Diurese, und andere Nebenwirkungen. Große Guarana Dosen kann dazu führen, Kopfschmerzen, Angst, Unruhe, Klingeln in den Ohren, Schmerzen beim Urinieren, Magenkrämpfe und unregelmäßiger Herzschlag. Menschen, die Guarana nehmen regelmäßig erleben Koffein Entzugserscheinungen, wenn sie ihre übliche Menge zu verringern; Guarana ist wahrscheinlich, unsicher und sogar tödlich aufgrund seiner Koffeingehalt, wenn sie in sehr hohen Dosen durch den Mund oder injiziert genommen. Die tödliche Dosis von Koffein wird geschätzt, 10-14 Gramm (150-200 mg pro Kilogramm, die â € œtypicalâ € Mann wiegt etwa 70 Kilogramm, so dass eine tödliche Dosis von Koffein für diesen Mann wäre 10,500-14,000 mg) zu sein. Dies ist eine ziemlich hohe Dosis. Bedenken Sie, dass eine Tasse Kaffee von 95 bis 200 mg Koffein enthält. Allerdings können schwere Vergiftungen bei Dosen von weniger als 150 bis 200 mg pro Kilogramm auftreten in Abhängigkeit von einer Koffein Empfindlichkeit oder das Rauchverhalten des Individuums, dem Alter und vor Koffein Gebrauch; Besondere Vorsichtsmaßnahmen und Warnungen: Schwangerschaft und der Stillzeit: Guarana ist VIELLEICHT SAFE für Schwangere und stillenden Frauen, wenn sie in Mengen gefunden häufig in Lebensmitteln genommen. Wenn Sie schwanger sind oder stillen, Guarana sollte aufgrund der Koffeingehalt mit Vorsicht eingenommen werden. Kleine Mengen sind wahrscheinlich nicht schädlich. Allerdings Guarana in hohen Dosen von Mund zu nehmen ist nicht ungefährlichen. Der Konsum von mehr als 200 mg hat zu einem erhöhten Risiko für eine Fehlgeburt und andere negative Auswirkungen in Verbindung gebracht worden; Angst: Das Koffein in Guarana könnten Gefühle der Angst noch schlimmer machen; Blutungsstörungen: Es gibt einige Hinweise darauf, dass das Koffein in Guarana könnte Blutungsstörungen verschlimmern, obwohl dies bei Menschen berichtet worden ist. Wenn Sie eine Störung der Blutgerinnung haben, überprüfen Sie mit Ihrem Arzt vor dem Start Guarana; Diabetes: Einige Untersuchungen zeigen, dass das Koffein in Guarana die Art, wie Menschen mit Diabetes Prozess Zucker (Glukose) beeinflussen kann und die Blutzuckerkontrolle erschweren. Es gibt auch einige interessante Forschung, die Koffein schlägt vor, können die Warnzeichen von niedrigem Blutzucker bei Patienten mit Typ-1-Diabetes zu verbessern. Einige Studien zeigen, dass die Symptome von niedrigem Blutzucker sind intensiver, wenn sie in Abwesenheit von Koffein zu starten, aber wie niedriger Blutzucker weiter, Symptome sind größer mit Koffein. Dies könnte die Fähigkeit der Diabetes-Patienten erhöhen zu erkennen und zu niedrigen Blutzucker zu behandeln. Allerdings ist der Nachteil, dass Koffein tatsächlich die Anzahl der Low-Zucker Episoden erhöhen könnten. Wenn Sie Diabetes haben, mit Ihrem Arzt sprechen, bevor Guarana beginnen; Durchfall. Guarana enthält Koffein. Das Koffein in Guarana, vor allem, wenn in großen Mengen eingenommen wird, kann Durchfall verschlimmern; Das Reizdarmsyndrom (IBS): Guarana enthält Koffein. Das Koffein in Guarana, vor allem wenn sie in großen Mengen eingenommen, Durchfall verschlimmern können und möglicherweise Symptome von IBS verschlechtern; Herzkrankheit: Das Koffein in Guarana kann dazu führen, unregelmäßiger Herzschlag bei bestimmten Menschen. Mit Vorsicht verwenden; Hoher Blutdruck: Unter Guarana kann Blutdruck bei Menschen mit hohem Blutdruck aufgrund seiner Koffeingehalt zu erhöhen. Allerdings könnte dieser Effekt weniger bei Menschen, die regelmäßig Kaffee-Trinker sind oder auf andere Weise Koffein auf einer regelmäßigen Basis zu verwenden; Glaucoma: Das Koffein in Guarana erhöht den Druck im Inneren des Auges. Der Anstieg tritt innerhalb von 30 Minuten und dauert mindestens 90 Minuten nach dem koffeinhaltigen Getränke zu trinken; Osteoporose: Das Koffein in Guarana Kalzium aus dem Körper über die Nieren spülen kann. Dieses Kalzium-Verlust könnte helfen, Knochen zu schwächen. Um dieses Problem zu minimieren, sollten Sie nicht mehr als 300 mg Koffein pro Tag. Einnahme von Kalziumpräparaten kann auch diese Kalziumverluste ausgleichen helfen. Postmenopausalen Frauen, die ein genetisches Problem haben, das beeinflusst, wie Vitamin D vom Körper verwendet wird, sollte Koffein mit Vorsicht zu verwenden.
Stimulanzien wie Amphetamine beschleunigen das Nervensystem auf. Durch die Beschleunigung des Nervensystems, stimulierende Medikamente können Sie nervös fühlen und Ihre Herzfrequenz erhöhen. Das Koffein in Guarana könnte auch das Nervensystem zu beschleunigen. Unter Guarana zusammen mit Stimulanzien kann zu ernsthaften Problemen wie erhöhte Herzfrequenz und Bluthochdruck führen. Vermeiden Sie Stimulanzien zusammen mit Koffein.
Stimulanzien wie Kokain beschleunigen das Nervensystem auf. Durch die Beschleunigung des Nervensystems, stimulierende Medikamente können Sie nervös fühlen und Ihre Herzfrequenz erhöhen. Das Koffein in Guarana könnte auch das Nervensystem zu beschleunigen. Unter Guarana zusammen mit Stimulanzien kann zu ernsthaften Problemen wie erhöhte Herzfrequenz und Bluthochdruck führen. Vermeiden Sie Stimulanzien zusammen mit Koffein.
Stimulierende Medikamente beschleunigen das Nervensystem auf. Koffein (enthalten in Guarana) und Ephedrin sind beide Stimulanzien. Unter Guarana zusammen mit Ephedrin könnte zu viel Stimulation verursachen und manchmal schwere Nebenwirkungen und Herzprobleme. Nehmen Sie nicht koffeinhaltige Produkte und Ephedrin zugleich.
Guarana enthält Koffein. Das Koffein in Guarana könnte der Block Wirkungen von Adenosin (Adenocard). Adenosine (Adenocard) wird oft von Ärzten verwendet, um einen Test auf dem Herzen zu tun. Dieser Test ist ein Herz-Stress-Test genannt. Stoppen Sie raubend Guarana oder andere koffeinhaltige Produkte mindestens 24 Stunden vor einer Herzbelastungstest.
Der Körper bricht Koffein loszuwerden, um es zu bekommen. Einige Antibiotika könnten verringern, wie schnell der Körper Koffein bricht. Die Einnahme dieser Antibiotika zusammen mit Guarana kann das Risiko von Nebenwirkungen wie Nervosität, Kopfschmerzen, erhöhte Herzfrequenz und andere Nebenwirkungen erhöhen; Einige Antibiotika, die abnehmen, wie schnell der Körper bricht Koffein enthalten Ciprofloxacin (Cipro), Enoxacin (Penetrex), Norfloxacin (Chibroxin, Noroxin), sparfloxacin (Zagam), Trovafloxacin (Trovan) und Grepafloxazin (Raxar).
Guarana enthält Koffein. Der Körper bricht Koffein loszuwerden, um es zu bekommen. Cimetidin (Tagamet) abnehmen kann, wie schnell Ihr Körper Koffein bricht. Unter Cimetidin (Tagamet) zusammen mit Guarana könnte die Chance von Koffein Nebenwirkungen wie Nervosität, Kopfschmerzen, schneller Herzschlag und andere erhöhen.
Der Körper bricht Clozapin (Clozaril) davon zu befreien. Das Koffein in Guarana scheint zu verringern, wie schnell der Körper bricht Clozapin (Clozaril). Unter Guarana zusammen mit Clozapin (Clozaril) können die Wirkungen und Nebenwirkungen von Clozapin (Clozaril) erhöhen.
Guarana enthält Koffein. Das Koffein in Guarana könnte der Block beeinflusst von Dipyridamol (Persantin). Dipyridamol (Persantin) wird oft von Ärzten verwendet, um einen Test auf dem Herzen zu tun. Dieser Test ist ein Herz-Stress-Test genannt. Stoppen Sie raubend Guarana oder andere koffeinhaltige Produkte mindestens 24 Stunden vor einer Herzbelastungstest.
Der Körper bricht Koffein loszuwerden, um es zu bekommen. Disulfiram (Antabuse) abnehmen kann, wie schnell der Körper von Koffein entledigt. Unter Guarana zusammen mit Disulfiram (Antabuse) (das Koffein enthält) könnte die Wirkungen und Nebenwirkungen von Koffein einschließlich jitteriness, Hyperaktivität, Reizbarkeit und andere erhöhen.
Der Körper bricht das Koffein in Guarana nach unten davon loszuwerden. Östrogene abnehmen kann, wie schnell der Körper bricht Koffein. Unter Guarana zusammen mit Östrogenen können Zittern, Kopfschmerzen, schneller Herzschlag und andere Nebenwirkungen verursachen. Wenn Sie nehmen Östrogene beschränken Sie Ihre Aufnahme von Koffein; Einige Östrogen Tabletten schließen konjugierte equine Estrogene (Premarin), Ethinylestradiol, Estradiol und andere.
Der Körper bricht das Koffein in Guarana nach unten davon loszuwerden. Fluvoxamine (Luvox) abnehmen kann, wie schnell der Körper Koffein bricht. Unter Guarana zusammen mit Fluvoxamin (Luvox) könnte zu viel Koffein im Körper verursachen, und die Wirkungen und Nebenwirkungen von Koffein erhöhen.
Sie Körper auf natürliche Weise wird von Lithium befreien. Das Koffein in Guarana erhöhen kann, wie schnell sich Ihr Körper von Lithium entledigt. Wenn Sie Produkte nehmen, die Koffein und Sie nehmen Lithium enthalten, zu stoppen langsam Koffein Produkte nehmen. Stoppen zu Koffein schnell die Nebenwirkungen von Lithium zu erhöhen.
Guarana enthält Koffein. Koffein kann den Körper zu stimulieren. Einige Medikamente gegen Depressionen verwendet wird, kann auch den Körper zu stimulieren. Unter Guarana mit diesen für Depressionen Medikamente kann zu schweren Nebenwirkungen wie schneller Herzschlag, Bluthochdruck, Nervosität und andere verursachen; Einige dieser Medikamente für Depression verwendet werden, umfassen phenelzine (Nardil), Tranylcypromin (Parnate) und andere.
Guarana enthält Koffein. Koffein könnte verlangsamen Blutgerinnung. Unter Guarana zusammen mit Medikamenten, die auch langsam Blutgerinnung könnten die Chancen von Quetschungen und Blutungen erhöhen; Einige Medikamente, die langsam Blutgerinnung gehören Aspirin, Clopidogrel (Plavix), Diclofenac (Voltaren, Cataflam, andere), Ibuprofen (Advil, Motrin, andere), Naproxen (Anaprox, Naprosyn, andere), Dalteparin (Fragmin), Enoxaparin (Lovenox) Heparin, Warfarin (Coumadin) und andere.
Stimulanzien wie Nikotin beschleunigen das Nervensystem auf. Durch die Beschleunigung des Nervensystems, stimulierende Medikamente können Sie nervös fühlen und Ihre Herzfrequenz erhöhen. Das Koffein in Guarana könnte auch das Nervensystem zu beschleunigen. Unter Guarana zusammen mit Stimulanzien kann zu ernsthaften Problemen wie erhöhte Herzfrequenz und Bluthochdruck führen. Vermeiden Sie Stimulanzien zusammen mit Koffein.
Die stimulierende Wirkung des Koffeins in Guarana können die Schlaf-produzierenden Block Effekte von Pentobarbital.
Das Koffein in Guarana kann den Körper zu stimulieren. Phenylpropanolamine können auch den Körper zu stimulieren. Unter Guarana zusammen mit Phenylpropanolamin kann dazu führen, zu viel Stimulation und Erhöhung Herzschlag, Blutdruck und verursachen Nervosität.
Der Körper bricht Riluzol (Rilutek) zu es loszuwerden. Unter Guarana abnehmen kann, wie schnell der Körper bricht Riluzol (Rilutek) und die Wirkungen und Nebenwirkungen von Riluzol erhöhen.
Guarana enthält Koffein. Koffein funktioniert ähnlich wie Theophyllin. Koffein kann auch abnehmen, wie schnell der Körper wird von Theophyllin befreien. Unter Guarana zusammen mit Theophyllin kann die Wirkungen und Nebenwirkungen von Theophyllin erhöhen.
Der Körper bricht das Koffein in Guarana nach unten davon loszuwerden. Verapamil (Calan, Covera, Isoptin, Verelan) abnehmen kann, wie schnell der Körper von Koffein entledigt. Unter Guarana zusammen mit Verapamil (Calan, Covera, Isoptin, Verelan) kann das Risiko von Koffein Nebenwirkungen wie Nervosität, Kopfschmerzen und erhöhtem Herzschlag erhöhen.
Der Körper bricht das Koffein in Guarana nach unten davon loszuwerden. Alkohol kann zu verringern, wie schnell der Körper Koffein bricht. Unter Guarana zusammen mit Alkohol kann dazu führen, zu viel Koffein in den Blutkreislauf und Koffein Nebenwirkungen wie Nervosität, Kopfschmerzen und schneller Herzschlag.
Der Körper bricht das Koffein in Guarana nach unten davon loszuwerden. Geburtenkontrolle Pillen abnehmen kann, wie schnell der Körper Koffein bricht. Unter Guarana zusammen mit Geburtenkontrolle Pillen können Zittern, Kopfschmerzen, schneller Herzschlag verursachen und andere Nebenwirkungen; Einige Antibabypillen enthalten Ethinylestradiol und Levonorgestrel (Triphasil), Ethinylestradiol und Norethindron (Ortho-Novum 1/35, Ortho-Novum 7/7/7) und andere.
Guarana enthält Koffein. Der Körper bricht Koffein loszuwerden, um es zu bekommen. Fluconazol (Diflucan) könnte abnehmen, wie schnell der Körper zusammen mit Fluconazol (Diflucan) Koffein Einnahme von Guarana entledigt sich die Gefahr von Koffein Nebenwirkungen wie Nervosität, Angst und Schlaflosigkeit erhöhen.
Guarana könnte Blutzucker erhöhen. Diabetes-Medikamente werden verwendet, um Blutzucker zu senken. Durch die Erhöhung der Blutzucker, Guarana könnte die Wirksamkeit von Diabetes-Medikamente verringern. Überwachen Sie Ihre Blutzucker eng. Die Dosis Ihres Diabetes-Medikamente könnte geändert werden müssen; Einige Medikamente verwendet für Diabetes sind Glimepirid (Amaryl), Glibenclamid (DiaBeta, Glynase PresTab, Mikronas), Insulin, Pioglitazon (Actos), Rosiglitazon (Avandia), Chlorpropamid (Diabinese), Glipizid (Glucotrol), Tolbutamid (Orinase) und andere .
Guarana enthält Koffein. Der Körper bricht Koffein loszuwerden, um es zu bekommen. Mexiletine (Mexitil) abnehmen kann, wie schnell der Körper Koffein bricht. Unter Mexiletin (Mexitil) zusammen mit Guarana könnte die Koffein Wirkungen und Nebenwirkungen von Guarana erhöhen.
Der Körper bricht Koffein (in Guarana enthalten ist) los zu bekommen. Terbinafin (Lamisil) abnehmen kann, wie schnell der Körper von Koffein entledigt und erhöhen das Risiko von Nebenwirkungen wie Nervosität, Kopfschmerzen, erhöhter Herzschlag, und andere Effekte.
Die geeignete Dosis von Guarana, hängt von verschiedenen Faktoren wie dem Alter des Benutzers, der Gesundheit und verschiedenen anderen Bedingungen. Zu diesem Zeitpunkt gibt es nicht genügend wissenschaftliche Informationen einen geeigneten Bereich von Dosen für Guarana zu bestimmen. Denken Sie daran, dass natürliche Produkte sind nicht immer unbedingt sicher und Dosierungen von Bedeutung sein können. Achten Sie darauf, relevante Richtungen auf den Produktetiketten zu folgen und fragen Sie Ihren Arzt oder Apotheker oder anderen Angehörigen des Gesundheitswesens vor dem Gebrauch.
Akinyinka, O. O., Sowunmi, A., Honeywell, R., und Renwick, A. G. Die Auswirkungen der akuten Malaria falciparum auf die Verfügbarkeit von Koffein und den Vergleich von Speichel und Plasma gewonnenen pharmakokinetischen Parameter bei erwachsenen Nigerianer. Eur.J Clin Pharmacol 200; 56 (2): 159-165.
Aldoori, W. H., Giovannucci, E. L., Stampfer, M. J., RIMM, E. B., Flügel, A. L., und Willett, W. C. Eine prospektive Studie von Alkohol, Rauchen, Koffein, und das Risiko von Zwolffingerdarmgeschwur bei Männern. Epidemiologie 199; 8 (4): 420-424.
Aldridge, A., Aranda, J. V. und Neims, A. H. Koffein den Stoffwechsel des Neugeborenen. Clin Pharmacol Ther 197; 25 (4): 447-453.
Alstott, R. L., Miller, A. J., und Forney, R. B. Bericht eines menschlichen Todesopfer aufgrund Koffein. J.Forensic Sci. 197; 18 (2): 135-137.
Antunes, E., Gordo, W. M., de Oliveira, J. F., Teixeira, C. E., Hyslop, S., und De, Nucci G. Die Lockerung der isolierten Kaninchen Schwellkörper durch die Kräutermedizin Catuama und seine Bestandteile. Phytother.Res. 200; 15 (5): 416-421.
Arditti, J., Bourdon, J. H., Spadari, M., de Haro, L., Richard, N., und Valli, M. [Ma Huang, von Nahrungsergänzungsmittel zu missbrauchen]. Acta Clin Belg.Suppl 200; (1): 34-36.
Arnold, M. E., Petros, T. V., Beckwith, B. E., Coons, G., und Gorman, N. Die Wirkungen von Koffein, Impulsivität und Sex auf Speicher für Wortlisten. Physiol Behav. 198; 41 (1): 25-30.
Arya, L. A., Myers, D. L., und Jackson, N. D. Dietary Koffeinkonsum und das Risiko für Detrusorinstabilität: eine Fall-Kontroll-Studie. Obstet.Gynecol. 200; 96 (1): 85-89.
Astrup, A., Toubro, S., Kanone, S., Hein, P., Breum, L., und Madsen, J. Caffeine: eine doppelblinde, placebo-kontrollierte Studie ihrer thermogene, Stoffwechsel- und Herz-Kreislauf-Effekte bei gesunden Probanden. Am.J.Clin.Nutr. 199; 51 (5): 759-767.
Avato, P., Pesante, M. A., Fanizzi, F. P., und Santos, C. A. Seed Ölzusammensetzung von Paullinia cupana var. sorbilis (Mart.) Ducke. Lipids 200; 38 (7): 773-780.
Baghkhani, L. und Jafari, M. Kardiovaskuläre Nebenwirkungen mit Guarana verbunden sind: Gibt es einen kausalen Effekt? J.Herb.Pharmacother. 200; 2 (1): 57-61.
Bak, A. A. und Grobbee, D. E. Koffein, Blutdruck und Blutfette. Am.J.Clin Nutr. 199; 53 (4): 971-975.
Bak, A. A. und Grobbee, D. E. Kaffee, Koffein und Hämostase: eine Überprüfung. Neth.J.Med. 199; 37 (5-6): 242-246.
Banner, W., Jr. und Czajka, P. A. Akute Koffein Überdosis bei Neugeborenen. Am.J Dis Child 198; 134 (5): 495-498.
Barrett-Connor, E., Chang, J. C., und Edelstein, S. L. Kaffee-assoziierten durch tägliche Milchkonsum Offset Osteoporose. Das Rancho Bernardo Study. JAMA 1-26-199; 271 (4): 280-283.
Strand, C. A., Bianchine, J. R., und Gerber, N. Die Ausscheidung von Koffein im Sperma von Männern: Die Pharmakokinetik und der Vergleich der Konzentrationen in Blut und Sperma. J Clin Pharmacol 198; 24 (2-3): 120-126.
Belliardo, F., Martelli, A., und Valle, M. G. HPLC-Bestimmung von Koffein und Theophyllin in Paullinia cupana Kunth (Guarana) und Cola spp. Proben. Z.Lebensm.Unters.Forsch. 198; 180 (5): 398-401.
Bempong DK, Houghton PJ und Steadman K. Der Xanthingehalt von Guarana und seine Zubereitungen. Int J Pharmacog 199; 31 (3): 175-181.
Bempong, D. K. und Houghton, P. J. Auflösung und Absorption von Koffein aus Guarana. J.Pharm.Pharmacol. 199; 44 (9): 769-771.
Benoni, H., Dallakian, P., und Taraz, K. Studien über das ätherische Öl aus Guarana. Z.Lebensm.Unters.Forsch. 199; 203 (1): 95-98.
Berube-Elternteil S, Pelletier C, Dore J und Tremblay A. Einfluss von verkapselten grünem Tee und Guarana-Extrakten eine Mischung aus Epigallocatechin-3-Gallat und Koffein auf 24 h Energieaufwand und Fettoxidation bei Männern enthält. Br J Nutr 200; 94 (3): 432-436.
Bikin D, Conrad KA und Mayersohn M. Mangel an Einfluss von Koffein und Aspirin auf Lithium-Eliminierung. Clin Res 198; 30 (2): 249A.
Blanchard, J. und Sawers, S. J. Vergleichende Pharmakokinetik von Koffein bei jungen und älteren Männern. J Pharmacokinet.Biopharm. 198; 11 (2): 109-126.
Blanchard, J. und Sawers, S. J. Die absolute Bioverfügbarkeit von Koffein im Menschen. Eur.J.Clin.Pharmacol. 198; 24 (1): 93-98.
Blanchard, J. Proteinbindung von Koffein bei jungen und älteren Männern. J Pharm.Sci 198; 71 (12): 1415-1418.
Boublik, J. H., Quinn, M. J., Clements, J. A., Herington, A. C., Wynne, K. N. und Funder, J. W. Kaffee enthält starke Opiat-Rezeptorbindungsaktivität. Natur 1-20-198; 301 (5897): 246-248.
Boutroy, M. J., Vert, P., Monin, P., Royer, R. J., und Royer-Morrot, M. J. Methylierungs von Theophyllin Koffein bei Frühgeborenen. Lancet 4-14-197; 1 (8120): 830.
Bowden, K. Isolation von Paullinia pinnata Linn. Material mit Wirkung auf den Frosch isoliert Herz. Bri.Pharm.Chemother. 196; 18: 173-174.
Boyle, C. A., Berkowitz, G. S., Livolsi, V. A., Ort, S., Merino, M. J., Weiss, C., und Kelsey, J. L. Koffeinkonsum und masthopatische Brusterkrankungen: eine Fall-Kontroll-Studie epidemiologischer. J.Natl.Cancer Inst. 198; 72 (5): 1015-1019.
Bracco, D., Ferrarra, J. M., Arnaud, M. J., Jequier, E., und Schutz, Y. Effekte von Koffein auf den Energiestoffwechsel, Herzfrequenz, und methylxanthine Stoffwechsel in schlanken und übergewichtigen Frauen. Am J Physiol 199; 269 (4 Pt 1): E671-E678.
Brice C und Smith A. Die Wirkung von Koffein auf die simulierten Fahr, subjektive Wachheit und nachhaltige Aufmerksamkeit. Hum Psychopharmacol Clin Exp 200; 16 (7): 523-531.
Brooks, P. G., Gart, S., Heldfond, A. J., Margolin, M. L., und Allen, A. S. Messung der Wirkung von Koffein Beschränkung auf masthopatische Brusterkrankungen: die Rolle der Grafik Stress telethermometry als objektive Monitor der Krankheit. J Reprod Med 198; 26 (6): 279-282.
Brown, C. A., Bolton-Smith, C., Woodward, M., und Tunstall-Pedoe, H. Kaffee und Tee Verbrauch und die Prävalenz der koronaren Herzkrankheit bei Männern und Frauen: Ergebnisse aus der Scottish Heart Health Study. J.Epidemiolmunity Gesundheit 199; 47 (3): 171-175.
Brown, S. L., Salive, M. E., Pahor, M., Foley, D. J., Corti, M. C., Langlois, J. A., Wallace, R. B., und Harris, T. B. Occult Koffein als eine Quelle von Schlafstörungen in einer älteren Bevölkerung. J.Am.Geriatr.Soc. 199; 43 (8): 860-864.
Bruce, M. S. und Lader, M. Koffein Enthaltung bei der Behandlung von Angststörungen. Psychol.Med. 198; 19 (1): 211-214.
Bryant CM, Dowell CJ und Fairbrother G. Eine Studie über die Auswirkungen von Koffein auf Frequenz, Dringlichkeit randomisiert und Dranginkontinenz. Neuro-Urologie & Urodynamics 200; 19 (4): 501-502.
Bullough, B., Hindi-Alexander, M., und Fetouh, S. Methylxanthines und masthopatische Brusterkrankungen: eine Studie von Korrelationen. Nurse Pract. 199; 15 (3): 36-4.
Bydlowski, S. P., D’Amico, E. A. und Chamone, D. A. Ein wässriger Extrakt aus Guarana (Paullinia cupana) nimmt das Thromboxan der Plättchen-Synthese. Braz.J.Med.Biol.Res. 199; 24 (4): 421-424.
Bydlowski, S. P., Yunker, R. L., und Subbiah, M. T. Eine neuartige Eigenschaft eines wässrigen Guarana Extrakt (Paullinia cupana): Hemmung der Thrombozytenaggregation in vitro und in vivo. Braz.J.Med.Biol.Res. 198; 21 (3): 535-538.
Caballero, T., Garcia-Ara, C., Pascual, C., Diaz-Pena, J. M. und Ojeda, A. Urtikaria durch Koffein induziert. J.Investig.Allergol.Clin Immunol. 199; 3 (3): 160-162.
Campos, A. R., Barros, A. I., Santos, F. A. und Rao, V. S. Guarana (Paullinia cupana Mart.) Bietet Schutz vor Magen von Ethanol und Indometacin in Ratten induzierten Läsionen. Phytother Res. 200; 17 (10): 1199-1202.
Carlson, M. und Thompson, R. D. Flüssigkeitschromatographisches Bestimmung von methylxanthines und Catechine in pflanzlichen Zubereitungen enthalten Guarana. J.AOAC Int. 199; 81 (4): 691-701.
Chamone, D. A., Silva, M. I., Cassaro, C., Bellotti, G., Massumoto, C. M. und Fujimura, A. Y. Guaraná (Paullinia cupana) hemmt die Aggregation in Vollblut. Thrombosis and Haemostasis 198; 58 (1): 474.
Chelsky, L. B., Cutler, J. E., Griffith, K., Kron, J., McClelland, J. H., und McAnulty, J. H. Koffein und ventrikuläre Arrhythmien. Ein elektro Ansatz. JAMA 11-7-199; 264 (17): 2236-2240.
Conlisk A und Galuska D. ist Koffein mit Knochenmineraldichte assoziiert bei jungen erwachsenen Frauen? JAMA 200; 285 (6): 713.
Curatolo, P. W. und Robertson, D. Die gesundheitlichen Folgen von Koffein. Ann.Intern.Med. 198; 98 (5 Pt 1): 641-653.
da Fonseca, C. A., Leal, J., Costa, S. S., und Leitao, A. C. Genotoxische und mutagene Wirkungen von Guarana (Paullinia cupana) in prokaryotischen Organismen. Mutat.Res. 199; 321 (3): 165-173.
Dalvi, R. R. Akute und chronische Toxizität von Koffein: eine Überprüfung. Vet Hum.Toxicol 198; 28 (2): 144-150.
Daniels, J. W., Mole, P. A., Shaffrath, J. D., und Stebbins, C. L. Wirkungen von Koffein auf den Blutdruck, Herzfrequenz, und Unterarmblutfluss während der dynamischen Bein ausüben. J.Appl.Physiol 199; 85 (1): 154-159.
Davis, R. H. Beeinflusst Koffeineinnahme intraokularen Druck ?. Ophthalmology 198; 96 (11): 1680-1681.
Dawber, T. R., Kannel, W. B., und Gordon, T. Kaffee und Herz-Kreislauf- Erkrankungen. Beobachtungen aus der Framingham-Studie. N Engl J Med 10-24-197; 291 (17): 871-874.
De Freitas, B. und Schwartz, G. Wirkungen von Koffein bei chronischen psychiatrischen Patienten. Am.J.Psychiatry 197; 136 (10): 1337-1338.
de Oliveira, JF, Avila, AS, Braga, AC, de Oliveira, MB, Boasquevisque, EM, Jales, RL, Cardoso, VN, und Bernardo-Filho, M. Wirkung von Extrakt von Heilpflanzen über die Kennzeichnung von Blutelemente mit Technetium-99m und auf die Morphologie der roten Blutkörperchen: I – Studie mit Paullinia cupana. Fitoterapia 200; 73 (4): 305-312.
Debrah, K., Haigh, R., Sherwin, R., Murphy, J., und Kerr, D. Wirkung von akuten und chronischen Coffein Gebrauch auf der zerebrovaskulären, kardiovaskuläre und hormonelle Antworten auf Orthostase bei gesunden Probanden. Clin Sci 199 (Colch.); 89 (5): 475-480.
Dimaio, V. J. und Garriott, J. C. Lethal Koffein-Vergiftung in einem Kind. Forensic Sci. 197; 3 (3): 275-278.
Dobmeyer, D. J., Stine, R. A., Leier, C. V., Greenberg, R., und Schaal, S. F. Die arrhythmogene Wirkung von Koffein bei Menschen. N.Engl.J.Med. 4-7-198; 308 (14): 814-816.
Drew AK und Dawson AH. Pflanzliche xtreme: akute Toxizität verbunden mit intravenöser Guarana [abstract]. Journal of Toxicology – Klinische Toxikologie 200; 38 (2): 235-236.
du, Boisgueheneuc F., Lannuzel, A., Caparros-Lefebvre, D., und De Broucker, T. [Hirninfarkt bei einem Patienten raubend Mahuang Extrakt und Guarana]. Presse Med 2-3-200; 30 (4): 166-167.
Dulloo, A. G. und Miller, D. S. Die thermogenen Eigenschaften von Ephedrin / methylxanthine Mischungen: Studien am Menschen. Int.J Obes. 198; 10 (6): 467-481.
Dulloo, A. G., Geissler, C. A., Horton, T., Collins, A., und Miller, D. S. Normale Koffeinkonsum: Einfluss auf die Thermogenese und täglichen Energieverbrauch in mageren und postobese menschlichen Freiwilligen. Am J Clin Nutr 198; 49 (1): 44-50.
Edelstein, B. A., Keaton-Brasted, C., und Burg, M. M. Wirkungen von Koffein-Entzug auf nächtliche Enuresis, Schlaflosigkeit und Verhaltensbeschränkungen. J.Consult Clin Psychol. 198; 52 (5): 857-862.
Eggertsen, R., Andreasson, A., Hedner, T., Karlberg, B. E. und Hansson, L. Wirkung von Kaffee auf ambulante Blutdruck bei Patienten mit Hypertonie behandelt. J.Intern.Med. 199; 233 (4): 351-355.
Eisig, J. N., Zaterka, S., Massuda, H. K., und Bettarello, Trinken A. Kaffee bei Patienten mit Zwölffingerdarmgeschwür und einer Kontrollpopulation. Scand J Gastroenterol. 198; 24 (7): 796-798.
Elkins, R. N., Rapoport, J. L., Zahn, T. P., Buchsbaum, M. S., Weingärtner, H., Kopin, I. J., Langer, D., und Johnson, C. Akute Wirkungen von Koffein in normalen präpubertären Jungen. Am.J.Psychiatry 198; 138 (2): 178-183.
Elta, G. H., Behler, E. M. und Colturi, T. J. Vergleich von Kaffeekonsum und Kaffee-induzierte Symptome bei Patienten mit Zwölffingerdarmgeschwür, nonulcer Dyspepsie, und normale Kontrollen. Am J Gastroenterol. 199; 85 (10): 1339-1342.
Ernster, VL, Mason, L., Goodson, WH, III, Sicheln, EA, Säcke, ST, Selvin, S., Dupuy, ME, Hawkinson, J., und Hunt, TK-Effekte von Koffein-freie Diät auf gutartige Brust Krankheit: eine randomisierte Studie. Surgery 198; 91 (3): 263-267.
Espinola, E. B., Dias, R. F., Mattei, R., und Carlini, E. A. Pharmakologische Aktivität von Guarana (Paullinia cupana Mart.) In Labortieren. J.Ethnopharmacol. 199; 55 (3): 223-229.
Fang, S., Sherwood, R. A., Gamsu, H. R., Marsden, J. T., Peters, T. J., und Greenough, A. Vergleich der Wirkungen von Theophyllin und Koffein auf die Serum-Konzentration Erythropoietin bei Frühgeborenen. Eur.J Pediatr. 199; 157 (5): 406-409.
Freestone, S. und Ramsay, L. E. Wirkung von Kaffee und Zigarettenrauchen auf den Blutdruck von unbehandeltem und Diuretika behandelt Patienten mit Hypertonie. Am.J.Med. 198; 73 (3): 348-353.
Freestone, S., Yeo, W. W., und Ramsay, L. E. Wirkung von Kaffee und Zigarettenrauchen auf den Blutdruck von Patienten mit beschleunigten (maligne) Hypertonie. J.Hum.Hypertens. 199; 9 (2): 89-91.
Fukumasu, H., Silva, T. C., Avanzo, J. L., Lima, C. E., Mackowiak, I. I., Atroch, A., Spinosa, H. D., Moreno, F. S., und Dagli, M. L. Chemopräventive Wirkung von Paullinia cupana Mart var. sorbilis, die Guarana, auf Maus Hepatokarzinogenese. Cancer Lett. 5-7-200;
Galduroz, J. C. und Carlini, E. A. Die Auswirkungen der langfristigen Verabreichung von Guarana auf der Erkenntnis der normalen, älteren Probanden. Sao Paulo Med.J. 199; 114 (1): 1073-1078.
Galduroz, J. C. und Carlini, Ede A. Akute Wirkungen des Cupana Paulinia “Guarana” auf der Erkenntnis von gesunden Probanden. Sao Paulo Med.J. 199; 112 (3): 607-611.
Gallerani, M., Zanotti, C., Menozzi, L., Montezemolo, A., Monetti, V. C. und Tola, M. R. Barbiturate, analgetische und Koffein-Entzug. Am.J.Emerg.Med. 199; 12 (5): 603-605.
Gancedo SQ, Freire P, Fernandez Rivas M, und et al. Urtikaria von Koffein. J Clin Allerg Immunol 199; 88: 680-681.
Garrett, B. E. und Griffiths, R. R. Physical Abhängigkeit erhöht die relativen Wirkungen von Koffein im Vergleich zu Placebo zu verstärken. Psychopharmacology (Berl) 199; 139 (3): 195-202.
Gilliland K und Bullock W. Koffein: Eine potenzielle Drogenmissbrauch. Adv Alkohol Subst Missbrauch 198; 3 (1-2): 53-73.
Glore, S. und Ricker, A. Trigeminusneuralgie: Fallstudie der Schmerz Aufhören mit einer Low-Koffein-Diät. J.Am.Diet.Assoc. 199; 91 (9): 1120-1121.
Grant, D. M., Tang, B. K. und Kalow, W. Variability in Koffein-Stoffwechsel. Clin Pharmacol Ther 198; 33 (5): 591-602.
Greden, J. F., Victor, B. S., Fontaine, P., und Lubetsky, M. Koffein Entzugskopfschmerz: eine klinische Profil. Psychosomatik 198; 21 (5): 411-418.
Greenstadt, L., Yang, L., und Shapiro, D. Koffein, psychische Belastung und das Risiko für Bluthochdruck: eine kulturübergreifende Replikation. Psychosom.Med 198; 50 (1): 15-22.
Griffiths, R. R. und Chausmer, A. L. Koffein als Modell Droge der Abhängigkeit: Neue Entwicklungen in Koffein-Entzug zu verstehen, das Koffein Abhängigkeitssyndrom und Koffein negative Verstärkung. Nihon Shinkei Seishin Yakurigaku Zasshi 200; 20 (5): 223-231.
Griffiths, R. R., Evans, S. M., Heishman, S. J., Preston, K. L., Sannerud, C. A., Wolf, B., und Woodson, P. P. Niedrig dosiertes Koffein körperliche Abhängigkeit beim Menschen. J Pharmacol Exp Ther 199; 255 (3): 1123-1132.
Haller, C. A., Jacob, P., und Benowitz, N. L. Kurzfristige metabolischen und hämodynamischen Wirkungen von Ephedra und Guarana-Kombinationen. Clin.Pharmacol.Ther. 200; 77 (6): 560-571.
Harris, S. S. und Dawson-Hughes, B. Koffein und Knochenverlust bei gesunden Frauen nach der Menopause. Am J Clin Nutr 199; 60 (4): 573-578.
Henman, A. R. Guarana (Paullinia cupana var sorbilis.): Ökologische und soziale Perspektiven auf eine wirtschaftliche Anlage des zentralen Amazonasbecken. J.Ethnopharmacol. 198; 6 (3): 311-338.
Heyden, S. und Muhlbaier, L. H. Prospektive Studie von “fibrocystic Brustkrankheit” und Koffeinkonsum. Surgery 198; 96 (3): 479-484.
Hinkle, P. E., Coffey, C. E., Weiner, R. D., Kresse, M., und Christison, C. Verwendung von Koffein Anfällen bei ECT zu verlängern. Am.J.Psychiatry 198; 144 (9): 1143-1148.
Hoffmann, F. L., Garcia-Cruz, C. H., Vinturim, T. M., und Pagnocca, F. C. Übersicht über die mikrobiologische Qualität von nicht-alkoholische Getränke mit Kohlensäure. Folia Microbiol (Praha) 199. 42 (3): 199-202.
Horst K, Buxton RE und Robinson WD. Die Wirkung der gewöhnlichen Nutzung des Kaffees von entkoffeinierten Kaffee auf den Blutdruck und bestimmte motorische Reaktionen von normalen jungen Männern. J Pharmacol Exp Ther 193; 52: 322-337.
Hughes, J. R., Higgins, S. T., Bickel, W. K., Hunt, W. K., Fenwick, J. W., Gulliver, S. B. und Mireault, G. C. Koffein Selbstverwaltung, Rückzug, und dessen negative Auswirkungen unter Kaffeetrinkern. Arch.Gen.Psychiatry 199; 48 (7): 611-617.
James, J. E. Chronische Wirkungen des gewöhnlichen Koffeinkonsum auf Labor- und ambulante Blutdruckwerte. J.Cardiovasc.Risk 199; 1 (2): 159-164.
James, J. E. Ist gewöhnlichen Koffein einen vermeidbaren kardiovaskulären Risikofaktor verwenden? Lancet 1-25-199; 349 (9047): 279-281.
Jee, S. H., He, J., Whelton, P. K., Suh, I., und Klag, M. J. Die Wirkung der chronischen Kaffee trinken auf den Blutdruck: eine Meta-Analyse von kontrollierten klinischen Studien. Hypertonie 199; 33 (2): 647-652.
Johnsen O, Eliasson R und Abdel-Kadar MM. Wirkung von Koffein auf die Motilität und den Metabolismus von humanen Spermatozoen. Andrologia 197; 6 (1): 53-58.
Kamimori, G. H., Somani, S. M., Knowlton, R. G., und Perkins, R. M. Die Auswirkungen von Übergewicht und Bewegung auf die Pharmakokinetik von Koffein in schlanken und übergewichtigen Probanden. Eur J Clin Pharmacol 198; 31 (5): 595-600.
Karacan, I., Thornby, J. I., Anch, M., Booth, G. H., Williams, R. L., und Salis, P. J. Schlafstörungen durch Kaffee und Koffein induzierte dosisabhängig. Clin Pharmacol Ther 197; 20 (6): 682-689.
Kawachi, I., Colditz, G. A. und Stein, C. B. Erhöht sich das Kaffeetrinken das Risiko einer koronaren Herzkrankheit? Ergebnisse einer Meta-Analyse. Br Herz J 199; 72 (3): 269-275.
Kendler, K. S. und Prescott, C. A. Aufnahme von Koffein, Toleranz und Entzug bei Frauen: a population-based Zwillingsstudie. Am.J.Psychiatry 199; 156 (2): 223-228.
Vergleich und die Interaktion mit Panax Ginseng: Kennedy, D. O., Haskell, C. F., Wesnes, K. A. und Scholey, A. B. kognitive Leistung bei menschlichen Probanden nach Gabe von Guarana (Paullinia cupana) Extrakt verbessert. Pharmacol Biochem Behav 200; 79 (3): 401-411.
Keuchel, I., Kohnen, R., und Lienert, G. A. Die Auswirkungen von Alkohol und Koffein auf Konzentration Testleistung. Arzneimittelforschung. 197; 29 (6): 973-975.
Khodesevick AP. Fatal Koffein-Vergiftung (Fall aus der Praxis). Farmakol Toksikol 195; 19 (suppl): 62.
Koczapski, A., Paredes, J., Kogan, C., Ledwidge, B., und Higenbottam, J. Wirkung von Koffein auf das Verhalten von schizophrenen Patienten stationär. Schizophr.Bull. 198; 15 (2): 339-344.
Kulkarni, P. B. und Dorand, R. D. Koffein Toxizität bei einem Neugeborenen. Pediatrics 197; 64 (2): 254-255.
Lane, J. D. und Phillips-Bute, B. G. Caffeine Deprivation wirkt Wachsamkeit Leistung und Stimmung. Physiol Behav. 199; 65 (1): 171-175.
Lane, J. D. und Williams, R. B., Jr. Kardiovaskuläre Wirkungen von Koffein und Stress in regelmäßigen Kaffeetrinker. Psychophysiology 198; 24 (2): 157-164.
Lane, J. D. Auswirkungen von kurzen caffeinated-Getränkeentzug auf die Stimmung, Symptome und Psychomotorik. Pharmacol Biochem.Behav 199; 58 (1): 203-208.
Lang, T., Degoulet, P., Aime, F., Fouriaud, C., Jacquinet-Salord, MC, Laprugne, J., Haupt, J., Oeconomos, J., Phalente, J., und Prades, A . die Beziehung zwischen Kaffeekonsum und Blutdruck: Analyse von 6321 Probanden in der Pariser Region. Am.J Cardiol. 12-1-198; 52 (10): 1238-1242.
Lawson, D. H., Jick, H., und Rothman, K. J. Kaffee und Tee Verbrauch und Brusterkrankungen. Surgery 198; 90 (5): 801-803.
Levinson, W. und Dunn, P. M. Nonassociation von Koffein und masthopatische Brusterkrankungen. Arch.Intern.Med. 198; 146 (9): 1773-1775.
Levy, M. und Zylber-Katz, E. Koffein den Stoffwechsel und Kaffee zuzuschreibenden Schlafstörungen. Clin Pharmacol Ther 198; 33 (6): 770-775.
Li-Neng Y, Greenstadt L und Shapiro D. Effekte von Koffein auf den Blutdruck: Eine interkulturelle Vergleich. Psychophysiology 198; 20: 457.
Lieberman, H. R. Die Wirkung von Ginseng, Ephedrin und Koffein auf die kognitive Leistung, Stimmung und Energie. Nutr Rev 200; 59 (4): 91-102.
Lubin, F., Ron, E., Wachs, Y., Schwarz, M., Funaro, M., und Shitrit, A. Eine Fall-Kontroll-Studie von Koffein und methylxanthines in gutartigen Brusterkrankungen. JAMA 4-26-198; 253 (16): 2388-2392.
Lucas, P. B., Pickar, D., Kelsoe, J., Rapaport, M., Pato, C., und Hommer, D. Auswirkungen der akuten Verabreichung von Koffein bei Patienten mit Schizophrenie. Biol.Psychiatry 7-1-199; 28 (1): 35-40.
Mace, J. Toxizität von Koffein. J Pediatr 197; 92 (2): 345-346.
Marshall, J., Graham, S., und Swanson, M. Koffeinkonsum und gutartige Brusterkrankungen: eine Fall-Kontroll-Vergleich. Am.J.Public Gesundheit 198; 72 (6): 610-612.
Marx, F. Analyse von Guaranasamen: II. Studien über die Zusammensetzung der Tanninfraktion. Zeitschrift für Lebensmittel Untersuchung und Forschung 199; 190 (5): 429-431.
Marx, F. und et al. Analyse von guaraná
Mattei, R., Dias, R. F., Espinola, E. B., Carlini, E. A. und Barros, S. B. Guarana (Paullinia cupana): toxische Wirkungen auf das Verhalten bei Labortieren und Antioxidantien-Aktivität in vitro. J.Ethnopharmacol. 199; 60 (2): 111-116.
Mayo, K. M., Falkowski, W., und Jones, C. A. Koffein: Anwendung und Wirkung in einem Langzeit psychiatrischen Patienten. Br.J.Psychiatry 199; 162: 543-545.
McManamy MC und Schube PG. Koffeinintoxikation: Bericht über einen Fall die Symptome, von denen einer Psychose betrug. New England Journal of Medicine 193; 215: 616-620.
Miura, T., Tatara, M., Nakamura, K., und Suzuki, I. Wirkung von Guarana auf Übung in normalen und epinephrininduzierter glykogenolytischen Mäuse. Biol.Pharm.Bull. 199; 21 (6): 646-648.
Moraes VLG, Santos LFM, Castro SB, Loureiro LH, Lima OA, Souza MLM, Yien LMK, Rossi-Bergmann B, und Costa SS. Die Hemmung der Lymphozyten-Aktivierung durch Extrakte und Fraktionen von Kalanchoe, Alternanthera, Paullinia und Mikania Arten. Phytomedizin 199; 1: 199-204.
Morano, A., Jimenez-Jimenez, F. J., Molina, J. A., and Antolin, M. A. Risk-factors for Parkinson’s disease: case-control study in the province of Caceres, Spain. Acta Neurol.Scand 199; 89(3):164-170.
Morton, J. F. Widespread tannin intake via stimulants and masticatories, especially guarana, kola nut, betel vine, and accessories. Basic Life Sci 199; 59:739-765.
Myers, M. G. and Harris, L. High dose caffeine and ventricular arrhythmias. Can.J Cardiol. 199; 6(3):95-98.
Myers, M. G., Harris, L., Leenen, F. H., and Grant, D. M. Caffeine as a possible cause of ventricular arrhythmias during the healing phase of acute myocardial infarction. Am.J Cardiol. 5-1-198; 59(12):1024-1028.
Nagesh, R. V. and Murphy, K. A., Jr. Caffeine poisoning treated by hemoperfusion. Am.J.Kidney Dis. 198; 12(4):316-318.
Neims AH, Bailey J, and Aldridge A. Disposition of caffeine during and after pregnancy. Clin Res 197; 27:236A.
Nussberger, J., Mooser, V., Maridor, G., Juillerat, L., Waeber, B., and Brunner, H. R. Caffeine-induced diuresis and atrial natriuretic peptides. J Cardiovasc.Pharmacol 199; 15(5):685-691.
Nyska, A., Murphy, E., Foley, J. F., Collins, B. J., Petranka, J., Howden, R., Hanlon, P., and Dunnick, J. K. Acute hemorrhagic myocardial necrosis and sudden death of rats exposed to a combination of ephedrine and caffeine. Toxicol.Sci. 200; 83(2):388-396.
O’Dea, J. A. Consumption of nutritional supplements among adolescents: usage and perceived benefits. Health Educ.Res. 200; 18(1):98-107.
Ooms, T. G., Khan, S. A., and Means, C. Suspected caffeine and ephedrine toxicosis resulting from ingestion of an herbal supplement containing guarana and ma huang in dogs: 47 cases (1997-1999). J Am Vet Med Assoc 1-15-200; 218(2):225-229.
Parsons, W. D. and Neims, A. H. Effect of smoking on caffeine clearance. Clin Pharmacol Ther 197; 24(1):40-45.
Parsons, W. D. and Neims, A. H. Prolonged half-life of caffeine in healthy tem newborn infants. J Pediatr. 198; 98(4):640-641.
Parsons, W. D. and Pelletier, J. G. Delayed elimination of caffeine by women in the last 2 weeks of pregnancy. Can.Med.Assoc.J 9-1-198; 127(5):377-380.
Phillips-Bute, B. G. and Lane, J. D. Caffeine withdrawal symptoms following brief caffeine deprivation. Physiol Behav. 12-31-199; 63(1):35-39.
Pincomb, G. A., Lovallo, W. R., McKey, B. S., Sung, B. H., Passey, R. B., Everson, S. A., and Wilson, M. F. Acute blood pressure elevations with caffeine in men with borderline systemic hypertension. Am.J Cardiol. 2-1-199; 77(4):270-274.
Pincomb, G. A., Lovallo, W. R., Passey, R. B., Whitsett, T. L., Silverstein, S. M., and Wilson, M. F. Effects of caffeine on vascular resistance, cardiac output and myocardial contractility in young men. Am.J Cardiol. 7-1-198; 56(1):119-122.
Pizziol, A., Tikhonoff, V., Paleari, C. D., Russo, E., Mazza, A., Ginocchio, G., Onesto, C., Pavan, L., Casiglia, E., and Pessina, A. C. Effects of caffeine on glucose tolerance: a placebo-controlled study. Eur.J Clin Nutr. 199; 52(11):846-849.
Pola, J., Subiza, J., Armentia, A., Zapata, C., Hinojosa, M., Losada, E., and Valdivieso, R. Urticaria caused by caffeine. Ann.Allergy 198; 60(3):207-208.
Prineas, R. J., Jacobs, D. R., Jr., Crow, R. S., and Blackburn, H. Coffee, tea and VPB. J Chronic.Dis 198; 33(2):67-72.
Reeves, R. R., Struve, F. A., and Patrick, G. Somatic dysfunction increase during caffeine withdrawal. J.Am.Osteopath.Assoc. 199; 97(8):454-456.
Rejent T, Michalek R, and Krajewski M. Caffeine fatality with coincident ephedrine. Bull Int Assoc Forensic Toxicol 198; 16:18-19.
Robelin, M. and Rogers, P. J. Mood and psychomotor performance effects of the first, but not of subsequent, cup-of-coffee equivalent doses of caffeine consumed after overnight caffeine abstinence. Behav.Pharmacol 199; 9(7):611-618.
Roberts, A. T., Jonge-Levitan, L., Parker, C. C., and Greenway, F. The effect of an herbal supplement containing black tea and caffeine on metabolic parameters in humans. Altern Med Rev 200; 10(4):321-325.
Robertson, D., Frolich, J. C., Carr, R. K., Watson, J. T., Hollifield, J. W., Shand, D. G., and Oates, J. A. Effects of caffeine on plasma renin activity, catecholamines and blood pressure. N.Engl.J Med. 1-26-197; 298(4):181-186.
Rogers, P. J. and Dernoncourt, C. Regular caffeine consumption: a balance of adverse and beneficial effects for mood and psychomotor performance. Pharmacol Biochem.Behav. 199; 59(4):1039-1045.
Rommelspacher, H. [Guarana]. Dtsch.Med.Wochenschr. 3-17-199; 120(11):384.
Rosenberg, L., Miller, D. R., Helmrich, S. P., Kaufman, D. W., Schottenfeld, D., Stolley, P. D., and Shapiro, S. Breast cancer and the consumption of coffee. Am.J.Epidemiol. 198; 122(3):391-399.
Rosengren, A. and Wilhelmsen, L. Coffee, coronary heart disease and mortality in middle-aged Swedish men: findings from the Primary Prevention Study. J Intern Med 199; 230(1):67-71.
Rosmarin, P. C., Applegate, W. B., and Somes, G. W. Coffee consumption and blood pressure: a randomized, crossover clinical trial. J.Gen.Intern.Med. 199; 5(3):211-213.
Roth JA, Ivy AC, and Atkinson AJ. Caffeine and “peptic” ulcer: relation of caffeine and caffeine-containing beverages to the pathogenesis, diagnosis and management of peptic ulcer. JAMA 194; 126:814-820.
Rowland D and Mace J. Caffeine (no-doz) poisoning in childhood. West J Med 197; 124:52-53.
Ryall JE. Caffeine and ephedrine fatality. Bull Int Assoc Forensic Toxicol 198; 17:13.
Salvadori, M. C., Rieser, E. M., Ribeiro Neto, L. M., and Nascimento, E. S. Determination of xanthines by high-performance liquid chromatography and thin-layer chromatography in horse urine after ingestion of Guarana powder. Analyst 199; 119(12):2701-2703.
Santa, Maria A., Lopez, A., Diaz, M. M., Munoz-Mingarro, D., and Pozuelo, J. M. Evaluation of the toxicity of guarana with in vitro bioassays. Ecotoxicol.Environ.Saf 199; 39(3):164-167.
Schlemmer RF, Heinze WJ, Asta CL, and et al. Caffeine potentiates phenylpropanolamine lethality but not motor behavior. Fed Proc 198; 43:572.
Schoenfeld, C., Amelar, R. D., and Dubin, L. Stimulation of ejaculated human spermatozoa by caffeine. A preliminary report. Fertil.Steril. 197; 24(10):772-775.
Shirlow, M. J. and Mathers, C. D. A study of caffeine consumption and symptom; indigestion, palpitations, tremor, headache and insomnia. Int.J.Epidemiol. 198; 14(2):239-248.
Shorofsky, M. A. and Lamm, R. N. Caffeine-withdrawal headache and fasting. N.Y.State J.Med. 197; 77(2):217-218.
Shum, S., Seale, C., Hathaway, D., Chucovich, V., and Beard, D. Acute caffeine ingestion fatalities: management issues. Vet.Hum.Toxicol. 199; 39(4):228-230.
Sicard, B. A., Perault, M. C., Enslen, M., Chauffard, F., Vandel, B., and Tachon, P. The effects of 600 mg of slow release caffeine on mood and alertness. Aviat.Space Environ.Med. 199; 67(9):859-862.
Silverman, K., Evans, S. M., Strain, E. C., and Griffiths, R. R. Withdrawal syndrome after the double-blind cessation of caffeine consumption. N.Engl.J.Med. 10-15-199; 327(16):1109-1114.
Smith, A. P., Kendrick, A. M., and Maben, A. L. Effects of breakfast and caffeine on performance and mood in the late morning and after lunch. Neuropsychobiology 199; 26(4):198-204.
Smits, P., Corstens, F. H., Aengevaeren, W. R., Wackers, F. J., and Thien, T. False-negative dipyridamole-thallium-201 myocardial imaging after caffeine infusion. J Nucl.Med. 199; 32(8):1538-1541.
Smits, P., Temme, L., and Thien, T. The cardiovascular interaction between caffeine and nicotine in humans. Clin Pharmacol Ther 199; 54(2):194-204.
Stein, M. A., Krasowski, M., Leventhal, B. L., Phillips, W., and Bender, B. G. Behavioral and cognitive effects of methylxanthines. A meta-analysis of theophylline and caffeine. Arch.Pediatr.Adolesc.Med. 199; 150(3):284-288.
Stensvold, I. and Tverdal, A. The relationship of coffee consumption to various self-reported cardiovascular events in middle-aged Norwegian men and women. Scand J Soc Med 199; 23(2):103-109.
Stensvold, I., Tverdal, A., and Foss, O. P. The effect of coffee on blood lipids and blood pressure. Results from a Norwegian cross-sectional study, men and women, 40-42 years. J Clin Epidemiol. 198; 42(9):877-884.
Stillner, V., Popkin, M. K., and Pierce, C. M. Caffeine-induced delirium during prolonged competitive stress. Am.J.Psychiatry 197; 135(7):855-856.
Sumbaev, V. V. and Rozanov, A. I. [Effect of caffeine on xanthine oxidase activity]. Ukr.Biokhim.Zh. 199; 69(5-6):196-200.
Sung, B. H., Lovallo, W. R., Whitsett, T., and Wilson, M. F. Caffeine elevates blood pressure response to exercise in mild hypertensive men. Am.J.Hypertens. 199; 8(12 Pt 1):1184-1188.
Sung, B. H., Whitsett, T. L., Lovallo, W. R., al’Absi, M., Pincomb, G. A., and Wilson, M. F. Prolonged increase in blood pressure by a single oral dose of caffeine in mildly hypertensive men. Am.J Hypertens. 199; 7(8):755-758.
Superko, H. R., Myll, J., DiRicco, C., Williams, P. T., Bortz, W. M., and Wood, P. D. Effects of cessation of caffeinated-coffee consumption on ambulatory and resting blood pressure in men. Am J Cardiol 4-15-199; 73(11):780-784.
Sutherland, D. J., McPherson, D. D., Renton, K. W., Spencer, C. A., and Montague, T. J. The effect of caffeine on cardiac rate, rhythm, and ventricular repolarization. Analysis of 18 normal subjects and 18 patients with primary ventricular dysrhythmia. Chest 198; 87(3):319-324.
Tassaneeyakul, W., Birkett, D. J., McManus, M. E., Tassaneeyakul, W., Veronese, M. E., Andersson, T., Tukey, R. H., and Miners, J. O. Caffeine metabolism by human hepatic cytochromes P450: contributions of 1A2, 2E1 and 3A isoforms. Biochem.Pharmacol 5-18-199; 47(10):1767-1776.
Tisdell R, Iacobucci M, and Snodgrass W. Caffeine poisoning in an adult: survival with a serum concentration of 400 mg/L and need for adenosine agonist antidotes. Vet Hum Toxicol 198; 28(5):492.
Tondo, L. and Rudas, N. The course of a seasonal bipolar disorder influenced by caffeine. J.Affect.Disord. 199; 22(4):249-251.
Tuomilehto, J., Tuomilehto-Wolf, E., Virtala, E., and LaPorte, R. Coffee consumption as trigger for insulin dependent diabetes mellitus in childhood. BMJ 3-10-199; 300(6725):642-643.
Van Dusseldorp, M., Smits, P., Lenders, J. W., Temme, L., Thien, T., and Katan, M. B. Effects of coffee on cardiovascular responses to stress: a 14-week controlled trial. Psychosom.Med. 199; 54(3):344-353.
Van Dusseldorp, M., Smits, P., Thien, T., and Katan, M. B. Effect of decaffeinated versus regular coffee on blood pressure. A 12-week, double-blind trial. Hypertension 198; 14(5):563-569.
Wald, A., Back, C., and Bayless, T. M. Effect of caffeine on the human small intestine. Gastroenterology 197; 71(5):738-742.
Walsh, I., Wasserman, G. S., Mestad, P., and Lanman, R. C. Near-fatal caffeine intoxication treated with peritoneal dialysis. Pediatr.Emerg.Care 198; 3(4):244-249.
Weckerle, C. S., Stutz, M. A., and Baumann, T. W. Purine alkaloids in Paullinia. Phytochemistry 200; 64(3):735-742.
White, B. C., Lincoln, C. A., Pearce, N. W., Reeb, R., and Vaida, C. Anxiety and muscle tension as consequences of caffeine withdrawal. Science 9-26-198; 209(4464):1547-1548.
Wrenn, K. D. and Oschner, I. Rhabdomyolysis induced by a caffeine overdose. Ann.Emerg.Med. 198; 18(1):94-97.
Yu, G., Maskray, V., Jackson, S. H., Swift, C. G., and Tiplady, B. A comparison of the central nervous system effects of caffeine and theophylline in elderly subjects. Br.J Clin Pharmacol 199; 32(3):341-345.
Abernethy DR, Todd EL. Wertminderung von Koffein-Clearance durch chronische Anwendung von niedrig dosiertem östrogenhaltigen oralen Kontrazeptiva. Eur J Clin Pharmacol 198; 28: 425-8.
Acheson KJ, Gremaud G, Meirim I, et al. Metabolic effects of caffeine in humans: lipid oxidation or futile cycling? Am J Clin Nutr 200; 79:40-6.
Akhtar S, Wood G, Rubin JS, et al. Effect of caffeine on the vocal folds: a pilot study. J Laryngol Otol 199; 113:341-5.
Ali M, Afzal M. Ein potenter Inhibitor von Thrombin stimulierte Thromboxan der Plättchen Bildung von nicht verarbeiteten Tee. Prostaglandine Leukot Med 198; 27: 9-13.
Academy of Pediatrics. The transfer of drugs and other chemicals into human milk. Pediatrics 200; 108:776-89.
Andersen T, Fogh J. Gewichtsverlust und verzögerte Magenentleerung nach einer Süd pflanzliches Präparat bei übergewichtigen Patienten. J Hum Nutr Diet 200; 14: 243-50.
Anderson BJ, Gunn TR, Holford NH, Johnson R. Caffeine overdose in a premature infant: clinical course and pharmacokinetics. Anaesth Intensive Care 199; 27:307-11.
Aqel RA, Zoghbi GJ, Trimm JR, et al. Wirkung von Koffein verabreicht intravenös auf intrakoronare Verabreichung von Adenosin-induzierte koronare Hämodynamik bei Patienten mit koronarer Herzkrankheit. Am J Cardiol 200; 93: 343-6.
Ardlie NG, Glew G, Schultz BG, Schwartz CJ. Die Hemmung und Umkehrung der Thrombozytenaggregation durch Methyl Xanthine. Thromb Diath Haemorrh 196; 18: 670-3.
Avisar R, Avisar E, Weinberger D. Wirkung von Kaffeekonsum auf den intraokularen Druck. Ann Pharmacother 200; 36: 992-5 ..
Bara AI, Gerste EA. Koffein für Asthma. Cochrane Database Syst Rev 200; 4: CD001112 ..
Bell-DG, Jacobs I, Ellerington K. Wirkung von Koffein und Ephedrin Einnahme auf anaeroben Trainingsleistung. Med Sci Sports Exerc 200; 33: 1399-403.
Benowitz NL, Osterloh J, Goldschlager N, et al. Massiver Katecholaminausschüttung von Koffein-Vergiftung. JAMA 198; 248: 1097-8.
Boozer CN, Nasser JA, Heymsfield SB, et al. An herbal supplement containing Ma Huang-Guarana for weight loss: a randomized, double-blind trial. Int J Obes Relat Metab Disord 200; 25:316-24.
Bourin M, Bougerol T, Guitton B, Broutin E. A combination of plant extracts in the treatment of outpatients with adjustment disorder with anxious mood: controlled study vs placebo. Fundam Clin Pharmacol 199; 11:127-32.
Bracken MB, Triche EW, Belanger K, et al. Association of maternal caffeine consumption with decrements in fetal growth. Am J Epidemiol 200; 157:456-66..
Breum L, Pedersen JK, Ahlstrom F, et al. Comparison of an ephedrine/caffeine combination and dexfenfluramine in the treatment of obesity. A double-blind multi-centre trial in general practice. Int J Obes Relat Metab Disord 199; 18:99-103.
Briggs GB, Freeman RK, Yaffe SJ. Drugs in Pregnancy and Lactation. 5. Aufl. Philadelphia, PA: Lippincott Williams & Wilkin; 1998.
Brown NJ, Ryder D, Niederlassung RA. Eine pharmakodynamische Wechselwirkung zwischen Koffein und Phenylpropanolamin. Clin Pharmacol Ther 199; 50: 363-71.
Cannon ME, Cooke CT, McCarthy JS. Caffeine-induced cardiac arrhythmia: an unrecognised danger of healthfood products. Med J Aust 200; 174:520-1.
Carbo M, Segura J, De la Torre R, et al. Wirkung von Chinolone auf Koffein Disposition. Clin Pharmacol Ther 198; 45: 234-40.
Carrillo JA, Benitez J. klinisch signifikanten pharmakokinetischen Wechselwirkungen zwischen Nahrungs Koffein und Medikamente. Clin Pharmacokinet 200; 39: 127-53.
Chen JF, Xu K, Petzer JP, et al. Neuroprotection by caffeine and A(2A) adenosine receptor inactivation in a model of Parkinson’s disease. J Neurosci 200; 21:RC143..
Chiu KM. Die Wirksamkeit von Kalzium auf die Knochenmasse bei postmenopausalen Frauen. J Gerontol A Biol Sci Med Sci 199; 54: M275-80.
Chou T. Wake up and smell the coffee. Caffeine, coffee, and the medical consequences. West-J Med 199; 157:544-53.
Dews PB, Curtis GL, Hanford KJ, O’Brien CP. Die Häufigkeit der Koffein-Entzug in einer populationsbasierten Umfrage und in einer kontrollierten, verblindeten Pilotversuch. J Clin Pharmacol 199; 39: 1221-1232.
Dews PB, O’Brien CP, Bergman J. Caffeine: Auswirkungen auf das Verhalten des Rückzugs und der damit zusammenhängende Fragen. Food Chem Toxicol 200; 40: 1257-1261.
DiPiro JT, Talbert RL, Yee GC, et a; eds. Pharmacotherapy: A pathophysiologic approach. 4th ed. Stamford, CT: Appleton & Lange, 1999.
Donadio V, Bonsi P, Zele I, et al. Myoglobinuria after ingestion of extracts of guarana, Ginkgo biloba and kava. Ginkgo biloba and kava. Neurol Sci 200; 21:124.
Dreher HM. The effect of caffeine reduction on sleep quality and well-being in persons with HIV. J Psychosom Res 200; 54:191-8..
Elektronische Code of Federal Regulations. Titel 21. Teil 182 – Stoffe als sicher allgemein anerkannt. Verfügbar unter: http://ecfr.gpoaccess.gov/cgi/t/text/text-idx?c=ecfr&sid= 786bafc6f6343634fbf79fcdca7061e1 & rgn = div5 & view = text & node = 21: 3.0.1.1.13 & IDNr = 21
Eskenazi B. Caffeine—filtering the facts. N Engl J Med 199; 341:1688-9.
FDA. Proposed rule: dietary supplements containing ephedrine alkaloids. Available at: www.verity.fda.gov (Accessed 25 January 2000).
Fernandes O, Sabharwal M, Smiley T, et al. Moderate to heavy caffeine consumption during pregnancy and relationship to spontaneous abortion and abnormal fetal growth: a meta-analysis. Reprod Toxicol 199; 12:435-44.
Ferrini RL, Barrett-Connor E. Aufnahme von Koffein und endogenen Sexualsteroidspiegel bei postmenopausalen Frauen. Das Rancho Bernardo Study. Am J Epidemiol 1996: 144: 642-4.
For Dieter, Nearly the Ultimate Loss. The Washington Post. Verfügbar um: http://www.washingtonpost/archive/politics/2000/03/19/for-dieter-nearly-the-ultimate-loss/c0f07474-489d-4f44-bc17-1f1367c956ae/ (Accessed 19 March 2000).
Forrest WH Jr, Bellville JW, Brown BW Jr. Die Wechselwirkung von Koffein mit Pentobarbital als Nacht hypnotisch. Anesthesiology 197; 36: 37-41.
Grandjean AC, Reimers KJ, Bannick KE, Haven MC. The effect of caffeinated, non-caffeinated, caloric and non-caloric beverages on hydration. J Am Coll Nutr 200; 19:591-600..
Greenway FL, Raum WJ, DeLany JP. The effect of an herbal dietary supplement containing ephedrine and caffeine on oxygen consumption in humans. J Altern Complement Med 200; 6:553-5.
Hagg S, Spigset O, Mjorndal T, Dahlqvist R. Wirkung von Koffein auf Clozapin Pharmakokinetik bei gesunden Probanden. Br J Clin Pharmacol 200; 49: 59-63.
Haller CA, Benowitz NL, Jacob P 3.. Die hämodynamische Wirkung von Ephedra freien Gewichtsverlust ergänzt beim Menschen. Am J Med 200; 118: 998-1003 ..
Haller CA, Benowitz NL. Unerwünschte kardiovaskuläre und das Zentralnervensystem Ereignisse im Zusammenhang mit Nahrungsergänzungsmittel mit Ephedra-Alkaloide. N Engl J Med 200; 343: 1833-8.
Haller CA, Jacob P 3., Benowitz NL. Pharmacology of ephedra alkaloids and caffeine after single-dose dietary supplement use. Clin Pharmacol Ther 200; 71:421-32.
Härtere S, Fuhr U, Staib AH, Wolff T. Ciprofloxacin-Koffein: ein Arzneimittel-Wechselwirkungen mit Sitz in vivo- und In-vitro-Untersuchungen. Am J Med 198; 87: 89S-91S.
Healy DP, Polk RE, Kanawati L, et al. Wechselwirkungen zwischen oralen Ciprofloxacin und Koffein bei gesunden Probanden. Antimicrob Agents Chemother 198; 33: 474-8.
Heseltine D, Dakkak M, woodhouse K, et al. The effect of caffeine on postprandial hypotension in the elderly. J Am Geriatr Soc 199; 39:160-4.
Hodgson JM, puddey IB, Burke V, et al. Auswirkungen auf den Blutdruck zu trinken grünen und schwarzen Tee. J Hypertens 199; 17: 457-63.
Holmgren P, Norden-Pettersson L, Ahlner J. Koffein Todesfälle – vier Fallberichte. Forensic Sci Int 200; 139: 71-3.
Horner NK, Lampe JW. Mögliche Mechanismen der Diät-Therapie für fibrocystic Brust Bedingungen zeigen unzureichende Beweise für die Wirksamkeit. J Am Diet Assoc 200; 100: 1368-1380.
Howell LL, Coffin VL, Spealman RD. Behavioral and physiological effects of xanthines in nonhuman primates. Psychopharmacology (Berl) 199; 129:1-14.
Infante S, Baeza ML, Calvo M, et al. Anaphylaxie aufgrund Koffein. Allergie-200; 58: 681-2.
Institut für Medizin. Koffein für die Sustainment of Mental Aufgabe Performance: Formulierungen für militärische Operationen. Washington, DC: National Academy Press, 2001. Verfügbar unter: http://books.nap.edu/books/0309082587/html/index.html.
Jefferson JW. Lithium-Tremor und Koffeinkonsum: zwei Fälle von weniger trinken und mehr schütteln. J Clin Psychiatry 198; 49: 72-3.
Joeres R, Klinker H, Heusler H, et al. Einfluss von Mexiletin auf Koffein-Eliminierung. Pharmacol Ther 198; 33: 163-9.
Juliano LM, Griffiths RR. Eine kritische Überprüfung der Koffein-Entzug: empirische Validierung von Symptomen und Anzeichen, Häufigkeit, Schweregrad und die damit verbundenen Funktionen. Psychopharmacology (Berl) 200; 176: 1-29.
Kamimori GH, Penetar DM, Headley DB, et al. Effect of three caffeine doses on plasma catecholamines and alertness during prolonged wakefulness. Eur J Clin Pharmacol 200; 56:537-44..
Keijzers GB, De Galan BE, Tack CJ et al. Koffein kann Insulinsensitivität bei Menschen verringern. Diabetes Care. 2002 Fe; 25: 364-9.
Klebanoff MA, Levine RJ, DerSimonian R, et al. Maternal serum paraxanthine, a caffeine metabolite, and the risk of spontaneous abortion. N Engl J Med 199; 341:1639-44.
Kleemola P, Jousilahti P, Pietinen P, et al. Coffee consumption and the risk of coronary heart disease and death. Arch Intern Med 200; 160:3393-400..
Kockler DR, McCarthy MW, Lawson CL. Anfallsaktivität und Teilnahmslosigkeit nach hydroxycut Einnahme. Pharmakotherapie 200; 21: 647-51 ..
Kynast-Gales SA, Massey LK. Wirkung von Koffein auf die zirkadiane Ausscheidung von Urin-Calcium und Magnesium. J Am Coll Nutr. 199; 13: 467-72.
See CR, Rosenberg DB, Gallant S, et al. Phenylpropanolamine erhöht die Plasma-Koffein Ebenen. Clin Pharmacol Ther 199; 47: 675-85.
Lane JD, Barkauskas CE, Surwit RS, Feinglos MN. Caffeine impairs glucose metabolism in type 2 diabetes. Diabetes Care 200; 27:2047-8.
Leson CL, McGuigan MA, Bryson SM. Koffein Überdosis in einem Jugendlichen männlichen Geschlechts. J Toxicol Clin Toxicol 198; 26: 407-15.
Lloyd T, Johnson-Rollings N, Eggli DF, et al. Knochenstatus bei postmenopausalen Frauen mit verschiedenen gewöhnlichen Koffein Aufnahme: eine Längsschnittuntersuchung. J Am Coll Nutr 200; 19: 256-61.
Mansi IA, Huang J. Rhabdomyolyse als Antwort auf Gewichtsverlust Kräutermedizin. Am J Med Sci 200; 327: 356-357.
Massey LK, Whiting SJ. Koffein, die Ausscheidung von Kalzium, Kalzium-Stoffwechsel und Knochen. J Nutr 199; 123: 1611-4.
Massey LK. Ist Koffein ein Risikofaktor für den Knochenverlust bei älteren Menschen? Am J Clin Nutr 200; 74: 569-70.
Mai DC, Jarboe CH, VanBakel AB, Williams WM. Auswirkungen von Cimetidin auf Koffein Disposition in Raucher und Nichtraucher. Clin Pharmacol Ther 198; 31: 656-61.
McGowan JD, Altman RE, Kanto WP Jr. Neonatal withdrawal symptoms after chronic maternal ingestion of caffeine. Süd-Med J 198; 81:1092-4..
Mester R, Toren P, Mizrachi I, et al. Koffein-Entzug steigert Lithium-Blutspiegel. Biol Psychiatry 199; 37: 348-50.
Nawrot P, Jordan S, Eastwood J, et al. Effects of caffeine on human health. Lebensmittel Addit Contam 200; 20:1-30.
Nehlig A, Debry G. Consequences on the newborn of chronic maternal consumption of coffee during gestation and lactation: a review. J Am Coll Nutr 199; 13:6-21..
Nix D, Zelenitsky S, Symonds W, et al. Die Wirkung von Fluconazol auf die Pharmakokinetik von Koffein in jungen und älteren Probanden. Clin Pharmacol Ther 199; 51: 183.
Nurminen ML, Niittynen L, Korpela R, Vapaatalo H. Kaffee, Koffein und Blutdruck: eine kritische Überprüfung. Eur J Clin Nutr 199; 53: 831-9.
Petrie HJ, Chown SE, Belfie LM, et al. Caffeine ingestion increases the insulin response to an oral-glucose-tolerance test in obese men before and after weight loss. Am J Clin Nutr 200; 80:22-8.
Pollock BG, Wylie M, Stapel JA, et al. Inhibition von Coffein Metabolismus durch Östrogen-Ersatztherapie bei postmenopausalen Frauen. J Clin Pharmacol 199; 39: 936-40.
Raaska K, Raitasuo V, Laitila J, Neuvonen PJ. Wirkung von koffeinhaltigen gegen entkoffeinierten Kaffee auf die Serum-Konzentrationen Clozapin bei hospitalisierten Patienten. Grund Clin Pharmacol Toxicol 200; 94: 13-8.
Rapuri PB, Gallagher JC, Kinyamu HK, Ryschon KL. Aufnahme von Koffein erhöht die Rate der Knochenschwund bei älteren Frauen und interagiert mit Vitamin-D-Rezeptor-Genotypen. Am J Clin Nutr 200; 74: 694-700.
Rees K, Allen D, Lader M. The influences of age and caffeine on psychomotor and cognitive function. Psychopharmacology (Berl) 199; 145:181-8.
Robinson LE, Savani S, Battram DS, et al. Caffeine ingestion before an oral glucose tolerance test impairs blood glucose management in men with type 2 diabetes. J Nutr 200; 134:2528-33.
Ross GW, Abbott RD, Petrovitch H, et al. Association of coffee and caffeine intake with the risk of parkinson disease. JAMA 200; 283:2674-9.
Sanderink GJ, Bournique B, Stevens J, et al. Die Beteiligung der menschlichen CYP1A Isoenzyme in den Stoffwechsel und Wechselwirkungen mit anderen Medikamenten von Riluzol in vitro. Pharmacol Exp Ther 199; 282: 1465-1472.
Savitz DA, Chan RL, Herring AH, et al. Caffeine and miscarriage risk. Epidemiology 200; 19:55-62.
Schechter MD, Timmons GD. Objectively measured hyperactivity–II. Caffeine and amphetamine effects. J Clin Pharmacol 198; 25:276-80..
Sinclair CJ, Geiger JD. Koffein Einsatz im Sport. Eine pharmakologische Bewertung. J Sports Med Phys Fitness 200; 40: 71-9.
Smith A. Einfluss von Koffein auf das menschliche Verhalten. Food Chem Toxicol 200; 40: 1243-1255.
Spinella M. Herbal Medicines and Epilepsy: The Potential for Benefit and Adverse Effects. Epilepsy Behav 200; 2(6):524-532.
Stanek EJ, Melko GP, Charland SL. Xanthine Interferenz mit Dipyridamol-Thallium-201 myokardialen Bildgebung. Pharmacother 199; 29: 425-7.
Stookey JD. The diuretic effects of alcohol and caffeine and total water intake misclassification. Eur J Epidemiol 199; 15:181-8.
Suleman A, Siddiqui NH. Haemodynamic and cardiovascular effects of caffeine. Medicine On Line Int J Medicine 2000. www.priory/pharmol/caffeine.htm (Accessed 14 April 2000).
The National Toxicology Program (NTP). Koffein. Center for the Evaluation of Risks to Human Reproduction (CERHR). Available at: http://cerhr.niehs.nih.gov/common/caffeine.html.
Tobias JD. Caffeine in the treatment of apnea associated with respiratory syncytial virus infection in neonates and infants. Süd-Med J 200; 93:297-304.
Under DA. Welche Medikamente sollten vor einem pharmakologischer oder Belastungstest stattfinden? Cleve Clin J Med 200; 69: 449-50.
Vahedi K, Domingo V, Amarenco P, Bousser MG. Der ischämische Schlaganfall in einem Sportler, der Mahuang verbraucht Extrakt und Kreatin-Monohydrat für Bodybuilding. J Neurol Neurosurg Psychiatr 200; 68: 112-3.
Vandeberghe K, Gillis N, Van Leemputte M, et al. Caffeine counteracts the ergogenic action of muscle creatine loading. J Appl Physiol 199; 80:452-7.
Wahllander A, Paumgartner G. Wirkung von Ketoconazol und Terbinafin auf die Pharmakokinetik von Koffein bei gesunden Probanden. Eur J Clin Pharmacol 198; 37: 279-83.
Wakabayashi K, Kono S, Shinchi K, et al. Gewöhnlicher Kaffeekonsum und Blutdruck: Eine Studie der Selbstverteidigung Beamten in Japan. Eur J Epidemiol 199; 14: 669-73.
Wallach J. Interpretation von Diagnosetests. Eine Zusammenfassung der Labormedizin. Fünfte e; Boston, MA: Little Brown, 1992.
Watson JM, Jenkins EJ, Hamilton P, et al. Einfluss von Koffein auf die Frequenz und die Wahrnehmung von Hypoglykämie bei freilebenden Patienten mit Typ 1 Diabetes. Diabetes Care 200; 23: 455-9.
Watson JM, Sherwin RS, Deary IJ et al. Die Dissoziation von Augmented-physiologischen, hormonelle und kognitive Reaktion auf eine Hypoglykämie mit anhaltendem Koffein Einsatz. Clin Sci (Lond) 200; 104: 447-54.
Wemple RD, Lamb DR, McKeever KH. Caffeine vs caffeine-free sports drinks: effects on urine production at rest and during prolonged exercise. Int J Sports Med 199; 18:40-6.
Weng X, Odouli R, Li DK. Maternal caffeine consumption during pregnancy and the risk of miscarriage: a prospective cohort study. Am J Obstet Gynecol 200; 198:279.e1-8.
Williams MH, Branch JD. Creatine supplementation and exercise performance: an update. J Am Coll Nutr 199; 17:216-34.
Winkelmayer WC, Stampfer MJ, Willett WC, Curhan GC. Gewöhnlicher Koffeinkonsum und das Risiko von Bluthochdruck bei Frauen. JAMA 200; 294: 2330-5.
Zheng XM, Williams RC. Serum Koffeingehalt nach 24-stündiger Enthaltung: klinische Auswirkungen auf Dipyridamol (201) Tl Myokardszintigrafie. J Nucl Med Technol 200; 30: 123-7.
Natural Medicines Comprehensive Database Consumer Version. siehe Natural Medicines Comprehensive Database Professional Version. ÂTherapeutic Forschung Fakultät 2009.
Kaffee intravenös
31. März 2011
#8 mandarinorange

In der vorletzten Woche von Frau Pimpinellas Frühlingslock-Projekt habe ich mal wieder in die Restekiste gegriffen und eine Neuauflage der sommerlichen Herz-Schlüsselanhänger gezaubert (die noch kleineren Reste verarbeite ich im Moment, die zeige ich Euch spätestens am Wochenende ;-)
Farblich passende Temperaturen versprechen die nächsten Tage zu bringen und viel mehr Impressionen in mandarinorange findet Ihr hier.
Nächste Woche gibt es die finale Farbe
30. März 2011
Buchthema: Kochen
29. März 2011
Klappe, die zweite.
27. März 2011
Zitronenkuchen.


26. März 2011
Hellblaues Vichykaro geht sowieso immer *find*
Gehen wir das Wochenende ganz ruhig an, streichen alle Termine, ignorieren standhaft den räudigen Dekozustand des Hauses (drinnen wie draußen) und lassen das Traumwetter weiter völlig ungenutzt verstreichen - zumindest, was Tochterklein und mich betrifft. Wir kränkeln hier so vor uns hin und werden nachher zum Trost vielleicht mal einen Kuchen zusammenschmurgeln.
Maximal, denn die neue Muss-Vorgabe für Frau Fluchten bei aufkommenden Erkältungen lautet ja: HINLEGEN *nerv*
25. März 2011
Meine Große ist ohne eine einzige löchrige Jeans durch ihre gesamte Kindergartenzeit gekommen (holt es allerdings jetzt als Schulkind nach ;-), deswegen bin ich jedesmal wieder fassungslos *g*
Ok, das können beide gut, den dieser Haushalt ist ein röhrenjeansloser und wird es auch bleiben - schließlich war ich ein Teenie der Achtziger und bin entsprechend traumatisiert *grusel*
Der Zeit- und Frusteinsatz, bei der aktuellen Mode eine akzeptable neue Hose zu finden, ist erfahrungsgemäß so groß, dass Reparieren eindeutig die schnellere Alternative war. Drum gab es ein Rettungspaket in Form von Schrägbandeinfassungen am Saum und doppellagigen Patches auf den Knien (noch ein unschlagbarer Vorteil von WEITEN Beinen, da kann man sowas nämlich aufnähen, ohne die Hosenbeine auftrennen zu müssen *g*), sicherheitshalber gleich wieder aus Jeansstoff, mit ein bißchen Kontrast.
Ich bin ein großer Fan der logo!-Kindernachrichten.
Meine Großen schreit ja gerne mal "hier", wenn es um Tagespolitik geht und so schauen wir die inzwischen täglich und ich bin immer wieder begeistert, wie die Macher es schaffen, auch hochkomplexe Tagesthemen verständlich zu erklären. Heute gibt es nach den regulären Nachrichten um 19.30 Uhr ein Special zum Thema Japan - vielleicht ist das ja für die ein oder andere von Euch interessant ;-)
24. März 2011
#7 korallenrot

22. März 2011
Der etwas andere Weg.
Seit Monaten schon will ich mir eine nähen, nie komme ich mal dazu.
Darum habe ich die Gelegenheit beim Schopf gepackt, als mialuna ein besonders schönes Exemplar im Zuge der Aktion "Sei ein Held für Lucas" zugunsten der DKMS versteigerte.
21. März 2011
Einfach, effektvoll, toll beschrieben und ganz schnell zu nähen.
20. März 2011

Klar - BACKEN :-) Zum Beispiel Zimtschnecken für die .
Ich glaube, der Tag wird mein Freund.
19. März 2011
Sonst wird es nachher doch ein Kerl, und dann?? *g*
18. März 2011

17. März 2011
#6 kirschblütenrosa

Wenn ich diesen Blick sehe, weiß ich sofort, dass alles gut wird :-)
16. März 2011
Immer weiter, immer weiter.
Die Basis ist ein schöner, dunkler Jeansstoff, garniert mit ein paar frühlingsfrischen (Vintage-)Schätzchen :-)
Aber türkis und meine Kamera, das geht ja einfach gar nicht zusammen - die Bilder werden immer so derartig kontrastarm *groll* Da muss ich mir dringend etwas überlegen.
15. März 2011
Ich habe nichts verstanden, aber ich hatte große Angst.
Eine Weile später bekam ich dieses Buch geschenkt. Es ist erschütternd, fesselnd, ich habe es in einem Rutsch gelesen.
Und ich habe es gehasst.
Wie man sieht, steht es immer noch in unserem Bücherschrank, aber ich bekomme Beklemmungen, wenn ich es nur in der Hand habe. Bis heute würde ich es nicht nochmal lesen wollen.
Die Angst von damals hat sich festgefressen und sie sitzt tief. Selten wird das so offenbar wie im Moment.
Geschichte wiederholt sich :(
Zumindest da bin ich guter Dinge.
Atomausstieg - qu'est-ce que c'est?
Frankreich hat eine der höchsten Kernenergiequoten der Welt, und ich erlebe in diesen Tagen dort zum ersten Mal überhaupt sowas wie einen Hauch von Atomdebatte.
Die Kühlturmwolken werde ich also vermutlich auch noch in den nächsten Jahrzehnten von meinem Balkon aus sehen und nur beten können, dass es bei den (unglaublich zahlreichen) angeblich harmlosen Störfällen bleibt. Ich will nicht irgendwann von einer Minute auf die andere mein Zuhause verlassen müssen und nie mehr wiederkommen dürfen :(
Ich kann es gar nicht in Worte fassen.
14. März 2011
Sitting, waiting, whishing.
So lange ich rumliege, geht es mir gut. Dank Betablockern kein Herzrasen mehr, aber leider auch keinen erwähnenswerten Kreislauf. Zwischendurch, wenn ich brennende Augen vom vielen Lesen habe, nähe ich immer mal ein halbes Stündchen. Geht auch gut. Was weiter gar nicht geht: mehr als 20 Schritte laufen, kochen, etwas hoch- oder runterheben, schimpfen, aufregen, Nachrichten gucken. Wird sofort mit Schnappatmung und schmerzhaftem Ziehen abgestraft.
Die Familie tut also so, als sei ich gar nicht anwesend und regelt alles alleine, und ich tue im Gegenzug so, als würde ich die Wäsche- und Krümelberge nicht bemerken ;-) Diese Woche habe ich aber tolle Oma-Hilfe, danach müssen wir mal sehen.
Indem man sich mit einem fiebrigen Infekt zum Beispiel nicht ordnungsgemäß ins Bett packt, sondern sich weiter dem Alltagsallerlei widmet. Oder mit einem entzündeten, fiebrigen Finger. Ich hatte bekanntlich beides zu bieten. Wenn man dann noch einen kleinen, olympiareifen Spurt quer über den Schulhof draufpackt, hat man richtig gute Chancen *schiefgrins*
Aber ich bin ja lernfähig - vermutlich liege ich zukünftig beim ersten Nasenjucken angststarr unter der Decke.
Meine arme Familie ;-)
12. März 2011
12 von 12 [MÄR 2011]
Wer noch alles mitgemacht hat, seht Ihr heute in Caros schöner neuer Liste.
Nach einem ausgelesenen Buch, einem leergesurften iPhone und stundenlanger ZDF-Beschallung habe ich nach Mitternacht allerdings einfach den Kopf in die Arme gelegt und geschlafen. .
Diagnose wie erwartet: Herzmuskelentzündung, gar nicht schön. Fühlt sich auch nicht so an, nach zehn Schritten oder Worten am Stück keuche ich wie nach einem wilden Sprint :( Böse!
Schnell persönliche Nachrichtensperre auferlegen, sowas ist nix für Herzpatienten *schluck*
Ganz entschleunigt und entspannt *ommmmmmmmh*
10. März 2011
#5 fliederlila

Ganz viele weitere Bilder in fliederlila findet Ihr hier in Frau Pimpis Liste.
Die noch ausstehenden Farben sind
Ich traue mich gar nicht zum Arzt, was der sagt, weiß ich eh schon - schonen, schonen, schonen.
Ich geh dann mal die Kinder verkaufen *schiefgrins*
Das freut mich riesig, ebenso wie die neuen Leser!
👑 @__jane___doe

But first. #coffee ☕ #weekend #vibe #breakfast #fitfa #fitnesslifestyle #fitnes #fit #fitnessmotivatio #fitnessgirl #fitgir #fitnessfreak #fitnessaddic #gainz #determinatio #motivation #instafitnes #instafit #fitspiratio #fitspo #strongnotskinn #sport #physiqu #aesthetic #girlswithmuscl #girlswholift
@__jane___doe : @stranger_than_everyone bei mir zumindest nicht 😋😁 - am besten die ganze Kaffeebohne intravenös 💉
This product uses the Instagram API but is not endorsed or certified by Instagram. All Instagram™ logos and trademarks displayed on this application are property of Instagram.
INK361 uses cookies to enhance your user experience. Learn more
Beiträge

Kaffee. Auch gerne Intravenös.
Wäre da nicht dieses Zugangs – Mimimi..
Schreibe etwas dazu
weitere Beiträge

ES IST SO SCHWER…
Es ist sehr schwer kein Klugscheisser zu sein, wenn alle anderen so unerträglich dumm sind. Facebook Twitter Google+ Pinterest Email WhatsAppSchreibe etwas. weiterlesen

HOCHSOMMER…
Stell dir vor es ist ende August in Deutschland, der Hochsommer kommt noch mal zurück und das einzige was Urlaub hat, ist. weiterlesen

DIREKT AUF DIE FRESSE
DIREKT AUF DIE FRESSE Facebook Twitter Google+ Pinterest Email WhatsAppSchreibe etwas dazu Kommentare weiterlesen

DESHALB KAFFEE…
Kaffee weil gute Tage nie mit Grünkohlsaft beginnen. Facebook Twitter Google+ Pinterest Email WhatsAppSchreibe etwas dazu Kommentare weiterlesen

KAUM EMPFANG
Kaum Handyempfang in der Berliner U-Bahn, aber der IS schafft es Bekennervideos in der Pampa aus Höhlen hochzuladen. Ich. weiterlesen

VORAUSPLANEN
Mein Freund findet es nicht gut, dass ich alles so vorausplane. Eigentlich ist er gar nicht mein Freund. Noch nicht. Facebook. weiterlesen

ABGESTUMPFT
Ich bin so abgestumpft. Mich kann man nur noch mit wahren Gefühlen in Verlegenheit bringen. Facebook Twitter Google+ Pinterest Email. weiterlesen

ICH KANNTE DIE BANDS
Ich bin so alt, ich kannte die Bands auf meinen Bandshirts noch. Facebook Twitter Google+ Pinterest Email WhatsAppSchreibe etwas dazu. weiterlesen

RESPEKTLOSIGKEIT
An der Kasse telefonieren, die Kassiererin nicht eines Blickes würdigen und ihr die EC Karte hinwerfen. Neues Level der Respektlosigkeit. Facebook Twitter. weiterlesen

TOTAL SÜSSE SCHUHE….
Jedes mal wenn eine Frau einem Mann „Total süsse Schuhe zeigt“ Ist das so, als würde der Hund sagen „Riech mal an. weiterlesen








Send this to a friend
Your email Recipient email
Cookies helfen uns dabei, SK-Dienste anzubieten, zu schützen und zu verbessern. Wenn du unsere Webseite weiterhin verwendest, stimmst du unserer Nutzungsbedingungen zu Weitere Informationen Weitere Informationen Akzeptieren
Die Cookie-Einstellungen auf dieser Website sind auf "Cookies zulassen" eingestellt, um das beste Surferlebnis zu ermöglichen. Wenn du diese Website ohne Änderung der Cookie-Einstellungen verwendest oder auf "Akzeptieren" klickst, erklärst du sich damit einverstanden.
kaffee intravenös, spritze mit kaffeebohnen, kaffee sucht, frei
- Preis
- Information
- Beschreibung
Einloggen oder anmelden! Um Ihre Fotos in Galerien anzuordnen, müssen Sie sich einloggen oder anmelden. Die Anmeldung ist gratis!
Einloggen oder anmelden! Um Ihre Fotos in Galerien anzuordnen, müssen Sie sich einloggen oder anmelden. Die Anmeldung ist gratis!
Wählen Sie Ihren MonatspackWählen Sie Ihr Abonnement
Unsere Monatspacks ermöglichen Ihnen den Download von hochauflösenden Fotos und Vektoren – überall, ganz einfach und mit nur einem Preis für alle Dateien.
Ungenutzte Downloads werden in den nächsten Monat übernommen, solange Ihr Monatspack aktiv ist oder verlängert wird.
Natürlich können Monatspacks bis zu 72 Stunden vor Verlängerung jederzeit gekündigt werden, daher ist diese Option auch dann noch perfekt für Sie, wenn Sie nur Stockbilder für einen Monat benötigen.
2,50 € / Bild in Größe M
2 € / Bild in Größe M
1,50 € / Bild in Größe M
1 € / Bild in Größe M
0,75 € / Bild in Größe M
0,50 € / Bild in Größe M
Einloggen oder anmelden! Um Ihre Fotos in Galerien anzuordnen, müssen Sie sich einloggen oder anmelden. Die Anmeldung ist gratis!
Das Bild "kaffee intravenös, spritze mit kaffeebohnen, kaffee sucht, frei" von ViennaFrame ist bei Fotolia lizenzfrei ab 1 Credit erhältlich (Credit ab 0,74 €).
Dieses Bild ist im JPEG-Format erhältlich und kann für sämtliche professionellen Zwecke und in verschiedenen Auflösungen heruntergeladen werden (bis zu 5.472 x 3.648 Pixel in 300 DPI).
Der Urheber dieses Bildes, ViennaFrame, hat außerdem 2 Bilder aus der gleichen Serie.
Um dieses Bild herunterzuladen, können Sie Fotolia Credits oder einen Monatspack kaufen oder ein Abonnement abschließen und von Preisen ab 0,16 € pro Bild profitieren.
Gleiche Serie
kaffee intravenös: spritze mit kaffeebonen liegt am tisch

kaffee intravenös: hand hält spritze mit kaffeebohnen, süchtig
Standard Lizenz
Mit der Standard Lizenz können Bilder für sämtliche illustrativen Zwecke in sämtlichen Medien verwendet werden.
Erweiterte Lizenz
Die Erweitere Lizenz gibt Ihnen alle Rechte der Standard Lizenz und darüber hinaus die Möglichkeit, unsere Dateien mehr als 500.000 Mal zu drucken und für Ihre eigenen Produkte zu verwenden. Eine Erweiterte Lizenz erlaubt es Ihnen sogar, Derivate oder Produkte für den Weiterverkauf oder Vertrieb herzustellen.
Finden Sie das perfekte Stockmedium für Ihr nächstes Kreativprojekt.
Sichern Sie sich 10 Adobe Stock Bilder zum Testen.
Fotolia ist jetzt Adobe Stock: Sie erhalten Zugang zu sämtlichen Fotolia Contents – und noch viel mehr!
Vielfältiger, fantastischer Content
Adobe Stock bietet eine riesige Bandbreite hervorragender Bilder, Videos, Vorlagen und 3D-Assets sowie die außergewöhnlichen Premium und Editorial Collections an.
Tief integriert mit Ihren bevorzugten Creative Cloud Apps
Arbeiten Sie in Ihren Designs mit Layoutbildern und lizenzieren Sie die High-Res-Versionen direkt in Photoshop CC, Illustrator CC, InDesign CC und weiteren Adobe Desktop Apps. Erleben Sie den nahtlosen Workflow!
Services
Hilfe

Nutzungsbedingungen/VerträgeDatenschutzrichtlinie © Fotolia 2017  AdChoices
AdChoices
Instenon
UND nstenon - ein Medikament, das die Durchblutung des Gehirns beeinflusst.
Pharmakologische Wirkung
Instenon - kombiniert bedeutet, Wirkstoffe, die Hexobendin sind, etamivan, etofillin.
Bei der Verwendung von instenon Rückgang Krämpfe, erweitert die Blutgefäße, verbessert die Stoffwechselvorgänge im Gehirn wird angeregt Vasomotorenzentrum scheint mild harntreibende Wirkung.
Es gibt positive Rezensionen Instenon, dass es die Gehirnfunktion beeinträchtigt, wenn der Blutfluss, Hypoxie, Ischämie verbessert.
Produktform
Instenon Retardtabletten mit dem Gehalt an Wirkstoffen: Hexobendin - 20mg, etamivan - 50 mg, etofillin - 60 mg.
Produzieren und zu Tabletten mit einem hohen Gehalt an Wirkstoffen (Instenon forte): Hexobendin - 60mg, etamivan - 100 mg, etofilin - 60 mg.
Auch die Freigabe des Arzneimittels in einer Lösung, die 10 mg Hexobendin, etamivan 50 mg, 100 mg etofillina.
Anwendung instenon zur Behandlung von ischämischem Schlaganfall, und posttraumatische Enzephalopathie dyscirculatory, Restsymptome nach Schlaganfall, Gefäß Dystonie, andere Erscheinungsformen der unzureichenden Blutversorgung des Gehirns zu empfehlen.
Gebrauchsanweisung instenon
Tabletten Instenon bestimmt für den internen Gebrauch, kann die Lösung intramuskulär, intravenös verabreicht werden.
Innerhalb Medikament ist in der Regel für die chronischen Formen der schlechte Blutzufuhr zum Gehirn (zerebrovaskuläre Insuffizienz) übernommen. Weisen Sie eine Tablette Instenon fort oder zwei Tabletten mit einer reduzierten Menge von Wirkstoffen - zwei oder drei p / Tag 3-4ned.
In akuten Ischämie, zerebrale Hypoxie intramuskulär, intravenös, ein Fläschchen (1 ml) 1-3 p / Tag für 3-5sut verabreicht. (Oder bis eine merkliche Verbesserung). Nach den Anweisungen Instenon Lösung im gleichen Verhältnis verdünnt: ein Fläschchen des Arzneimittels auf 200 ml Natriumchloridlösung oder 5% Glucose.
Nebeneffekte
Negative Bewertungen Instenon ist seine Toleranz nicht genug.
Es wurde festgestellt, dass mit der raschen Einführung des Medikaments intravenös (eine Ampulle sollte nicht weniger als drei Minuten verabreicht werden) erscheinen Tachykardie, Kopfschmerzen, Gesichtsrötung.
Kontra instenon
Nach den Anweisungen Instenon bei Epilepsie, Hirnblutung kontraindiziert, erhöhtem Hirndruck, in einem Zustand der erhöhte Erregbarkeit, wenn Anfälle.
Es gibt Fälle, wenn das Ziel instenon Schwangerschaft Placentarkreislauf vor der Geburt zu verbessern.
Die Notwendigkeit für die Verwendung des Medikaments in dieser Zeit gelöst positiv nur auf der Grundlage von fetalen Herzschlag EKG, Ultraschall, so dass wir nicht auf eigene Faust, ohne ein ärztliches Rezept zu Instenon in der Schwangerschaft (während der Stillzeit und kann Instenon nicht eingenommen werden).
Im Verlauf der Behandlung sehr vorsichtig in die Bewirtschaftungsmechanismen, die Aufmerksamkeit erfordern, am Straßenverkehr sein muss. Es sollte auch beachtet werden, dass unter dem Einfluss von Koffein verringert die therapeutische Wirkung des Medikaments (kann nicht in großen Mengen an Kaffee, Tee verwendet werden).
Pneumonie und lungenkrebs: symptome, diagnosen und behandlungen

Pneumonie und Lungenkrebs treten beide in den Lungen auf und teilen sich eine Anzahl von überlappenden Symptomen.
Pneumonie ist eine Lungenentzündung, die häufig durch Bakterien, ein Virus oder einen Pilz verursacht wird. Lungenkrebs ist ein schädlicher Tumor oft durch Rauchen Tabak verursacht.
Dieser Artikel wird diskutieren, wie Lungenkrebs und Lungenentzündung den Körper beeinflussen, wie jede Bedingung diagnostiziert, behandelt und ihre relativen Aussichten ist.
Überblick über Pneumonie und Lungenkrebs

Ein geschwächtes Immunsystem kann für sehr junge und ältere Menschen eine Pneumonie tödlich machen.
Was ist eine Lungenentzündung?
Die Nase und die Atemwege sind sehr effektiv, um zu verhindern, dass die Luftkeime in die Lunge gelangen. Keime, die eine Lungenentzündung verursachen, können manchmal durch diese Verteidigung rutschen oder sich von einem anderen Teil des Körpers ausbreiten, um die Lungen zu infizieren.
Die Keime, die eine Pneumonie verursachen, können aus einer Reihe von Bakterien, Viren, Pilzen oder bestimmten Chemikalien abgeleitet werden. Die Schwere einer Infektion variiert je nach ihrer Ursache.
Die häufigsten Arten von Pneumonie sind bakterielle Pneumonie und virale Pneumonie, die beide gleichzeitig auftreten können.
Wenn sich die Infektion auf den Boden der Lungen ausbreitet, füllen sich die winzigen Luftsäcke, die Sauerstoff in den Blutkreislauf bringen lassen, mit Flüssigkeit auf. Die Luftsäcke können dann nicht richtig funktionieren. Weniger Sauerstoff wird dann aus der Lunge übertragen und mehr Abfall Kohlendioxid bleibt im Umlauf.
Krebs wird durch eine Mutation in Zell-DNA produziert, die dazu führt, dass Zellen ungewöhnlich funktionieren und sich unkontrolliert vermehren. Diese Krebszellen können wachsen, um Tumore zu bilden, die die normale Körperfunktion stören.
Lungenkrebs ist die zweithäufigste Form von Krebs in den Vereinigten Staaten hinter Brustkrebs. Es kommt vor, wenn Krebszellen in einer oder beiden Lungen entstehen.
Es ist möglich, dass Zellen infolge normaler Alterung krebsartig werden, aber Lungenkrebs wird am häufigsten durch Umweltfaktoren verursacht.
Zwischen 80-90 Prozent der Lungenkrebs Fälle sind durch Rauchen Tabak verursacht. Die Krankheit kann auch durch die Exposition gegenüber anderen Chemikalien einschließlich Radon oder Asbest ausgelöst werden.
Wer ist am meisten gefährdet?
Sowohl Pneumonie als auch Lungenkrebs können bei jedem auftreten, aber einige Individuen sind anfälliger als andere, um eine dieser Bedingungen zu entwickeln.
Rauchtabak ist ein wichtiger Risikofaktor für die Entwicklung von Lungenkrebs. Längere Rauchzeiten erhöhen das Risiko erheblich.
Einzelpersonen, die ein geschwächtes Immunsystem haben, sind besonders anfällig für die Entwicklung einer Lungenentzündung. Deshalb sind die sehr jungen und älteren Menschen eher eine Lungenentzündung als andere Altersgruppen zu entwickeln.
Es ist auch der Grund, warum schätzungsweise 50-70 Prozent der Menschen mit Lungenkrebs ernsthafte Lungeninfektionen, wie Pneumonie, im Verlauf ihrer Krankheit entwickeln.
Darüber hinaus lassen die aggressiven Therapien, die zur Behandlung von Lungenkrebs eingesetzt werden, oft Menschen mit stark geschwächten Immunsystemen. Das heißt, sie sind:
- Weniger in der Lage zu verhindern, dass Keime in ihren Körper gelangen
- Nicht so gut ausgestattet, um Infektionen zu bekämpfen oder auf Medikamente zu reagieren
In diesen Fällen sind Infektionen ein ernstes Gesundheitsrisiko. Pneumonie ist derzeit der zweitgrößte Mörder von Lungenkrebspatienten nach den Krebsgeschwüren selbst.
Ein geschwächtes Immunsystem ist auch der Grund, warum Pneumonie besonders schwer und manchmal tödlich bei sehr jungen und älteren Menschen ist.

Husten und Kurzatmigkeit sind Symptome, die sowohl Lungenkrebs als auch Lungenentzündung gemeinsam sein können.
Erzählen von Lungenentzündung und Lungenkrebs auseinander kann manchmal schwierig sein, da es eine Überlappung von einigen der Symptome gibt. Typischerweise sind die Symptome von Lungenkrebs um so schwerer.
Überlappende Symptome von Lungenentzündung und Lungenkrebs sind:
- Husten: Bei Lungenkrebs neigt dies dazu, dass es länger anhaltend ist und mehrere Wochen andauert und sich schrittweise verschlechtert.
- Phlegm: Das ist meist dunkelrot, braun, gelb oder grün.
- Kurzatmigkeit: Das ist bei Lungenkrebs stärker als bei Lungenentzündung.
- Stachelnde Brustschmerzen: Diese werden beim Atmen oder Husten schlimmer.
- Müdigkeit: häufiger bei Lungenkrebs als bei Lungenentzündung.
- Appetitlosigkeit: Bei Lungenkrebs ist dies oft mit Gewichtsverlust verbunden.
- Keuchen: Weniger häufig bei beiden Bedingungen.
Zusätzliche häufige Symptome nur mit Pneumonie verbunden sind:
Weniger häufige Symptome nur mit Pneumonie verbunden sind:
- Kopfschmerzen
- Übelkeit oder Erbrechen
- Gelenk- oder Muskelschmerzen
- Verwechslung
Zusätzliche häufige Symptome nur mit Lungenkrebs assoziiert sind:
Weniger häufige Symptome nur mit Lungenkrebs assoziiert sind:
- Schwellung im Gesicht oder Hals
- Dauerhafte Schulter- oder Nackenschmerzen
- Schluckbeschwerden
- Eine heisere Stimme
- hohe Temperatur
- Veränderung in der Form der Fingerspitzen
Diagnosen und Behandlungen

Ein Röntgenbild kann zur Diagnose von Lungenentzündung und Lungenkrebs eingesetzt werden.
Diagnose einer Lungenentzündung kann eine körperliche Untersuchung, um auf geschwollene Drüsen, abnorme Atmung oder eine hohe Temperatur zu überprüfen. Eine Diagnose wird oft mit einer Blutprobe oder einem Röntgenbild bestätigt, um jegliche Flüssigkeitsansammlung in der Lunge zu zeigen.
Die Behandlung der Pneumonie variiert je nach Art der Lungenentzündung und der Gesundheit der Person. In den meisten Fällen kann die Lungenentzündung zu Hause mit viel Flüssigkeit, Ruhe und Medikamenten behandelt werden.
In schweren Fällen kann eine Krankenhausbehandlung erforderlich sein, so dass Flüssigkeiten und Antibiotika intravenös verabreicht werden können. Sauerstofftherapie oder Atemhilfe kann auch erforderlich sein.
Diagnose Lungenkrebs kann schwieriger sein. Ein Thorax-Röntgenbild kann eine schnelle und einfache Kontrolle, aber eine Computertomographie (CT) Scan ist notwendig, um die Diagnose zu bestätigen.
Wenn Lungenkrebs bestätigt wird, können weitere Tests durchgeführt werden, einschließlich einer Positronenemissionstomographie-CT (PET-CT) Scan, um alle Krebszellen zu lokalisieren.
Eine Biopsie wird auch durchgeführt, wobei eine kleine Gewebeprobe aus den Lungen entnommen und unter einem Mikroskop untersucht wird.
Häufig wird das Gewebe über eine kleine Röhre genommen, die die Lungen durch die Nase oder den Mund erreicht. Dieses Verfahren ist als Bronchoskopie bekannt.
Die Ergebnisse dieser Tests bestimmen die Art des Lungenkrebses, die Lage des Primärtumors und die Stufe, die die Krankheit erreicht hat.
Diese Informationen werden verwendet, um die effektivste Behandlung Ansatz nach Berücksichtigung der allgemeinen Gesundheit der Person zu erarbeiten.
Behandlungen zielen darauf ab, die Symptome zu heilen, zu kontrollieren oder zu lindern. Die verfügbaren Optionen reichen von grundlegenden chirurgischen Verfahren bis hin zur Chemotherapie oder Strahlentherapie je nachdem, wie stark der Zustand der Person ist.
Die Mehrheit der Pneumonie Fälle sind nicht als schwerwiegend, obwohl die Krankheit ist ernst.
Die Länge der Zeit Symptome können dauern hängt von der Gesundheit des Individuums und die Art der Lungenentzündung ist es.
Bakterielle Lungenentzündung Symptome werden in der Regel nach 1-3 Wochen weggehen. Mycoplasma Pneumonie kann 4-6 Wochen dauern, und virale Pneumonie kann noch länger dauern.
Wenn die Lungenentzündung unbehandelt bleibt, können lebenswichtige Organe wie Herz und Gehirn nicht genügend Sauerstoff erhalten. Die Folge davon kann Verwirrung, Koma, Herzinsuffizienz oder sogar Tod sein.
Die Aussichten für Lungenkrebs sind in der Regel eher schwerwiegend, unabhängig von der Behandlung.
Wenn der Krebs in einem frühen Stadium diagnostiziert wird, gibt es eine Chance, dass es chirurgisch entfernt werden kann, während es klein ist und sich nicht verbreitet hat. Das gibt eine gute Chance zur Erholung.
Allerdings sind viele Patienten mit Lungenkrebs diagnostiziert, nachdem der Krebs bereits verbreitet hat. In diesen Fällen ist das Entfernen von es unwahrscheinlich. Behandlungen konzentrieren sich stattdessen darauf, ihre Progression zu begrenzen und die Symptome zu lindern.
Beispiel 1:
8,4 g (0,28 Mol) Natriumhydrid (80%ig) werden in 150 ml abs. Toluol vorgelegt. Nach Zutropfen von 80 g (0,23 Mol) N-(2,6-Dichlorphenylacetyl)-piperidin-2-carbonsäureethylester in 400 ml abs. Toluol, erhitzt man 6 h unter Rückfluß. Unter Eisbadkühlung wurden 30 ml Ethanol zugetropft, der Ansatz im Vakuum einrotiert, der Rückstand in 1 N NaOH gelöst und das 3-(2,6-Dichlorphenyl)-1,5-tetramethylen-pyrrolidin-2,4-dion bei 0-20°C mit konzentrierter HCl gefällt. Das Produkt wird zur Reinigung mit Chloroform ausgekocht, anschließend wird n-Hexan zugesetzt und das ausgefallene, farblose Produkt abgesaugt.
Ausbeute: 40,5 g (59,1% d. Theorie) Fp. > 250°C.
Beispiel 2:
4,6 g (15 mmol) 3-(2,4,6-Trimethylphenyl)-1,5-tetramethylen-pyrrolidin-2,4-dion werden in 50 ml abs. THF suspendiert und mit 1,22 ml (15 mmol) abs. Pyridin und 2,54 ml (15 mmol) Ethyl-diisopropylamin versetzt. Dazu tropft man bei 0°-10°C 1,94 ml (15 mmol) 3-Chlorpivaloylchlorid gelöst in 5 ml abs. THF und rührt 30 Min. nach. Der Niederschlag wird abfiltriert, die Lösung im Vakuum einrotiert und der Rückstand an Kieselgel mit Cyclohexan/Essigester 1:1 chromatographiert.
Durch Kristallisation aus Ether/n-Hexan erhält man 3,93 g (70% der Theorie) 4-(3-Chlorpivaloyloxy)-3-(2,4,6-trimethylphenyl)-1,5-tetramethylen-3-pyrrolin-2-on von Schmp. 102°C.
Beispiel 3
4,47 g (15 mmol) 3-(2,4-Dichlorphenyl)-1,5-tetramethylenpyrrolidin-2,4-dion werden in 50 ml abs. THF mit 1,22 ml (15 mmol) abs. Pyridin versetzt. Bei 0°C-10°C werden 2,44 g (15 mmol) Chlorameisensäureethoxyethylester gelöst in 5 ml abs. THF zugetropft und 30 Min. nachgerührt. Nach Abfiltrieren des Niederschlages wird das Filtrat im Vakuum einrotiert, der Rückstand an Kieselgel mit Cyclohexan/Essigester 1:2 chromatographiert und aus Ether/n-Hexan kristallisiert.
Ausbeute: 5,2 g (83,7% der Theorie) 4-Ethoxyethyl-oxycarbonyloxy-3-(2,4-dichlorphenyl)-1,5-tetramethylen-3-pyrrolin-2-on vom Schmp. 80°C.
In entsprechender Weise zu den Herstellungsbeispielen und gemäß den allgemeinen Angaben zur Herstellung erhält man die in den folgenden Tabellen 1-3 formelmäßig aufgeführten 3-Aryl-pyrrolidin-2,4-dion(e)-Derivate der Formel (Ia) - (Ic).
Beispiel 256
2,57 g (10 mMol) 3-(2,4,6-Trimethyl-phenyl)-1,5-trimethylen-pyrrolidin-2,4-dion werden in 50 ml absoluten THF (Tetrahydrofuran) suspendiert und anschließend Dimethylamin durchgeleitet, bis die Gasaufnahme beendet ist. Nach dem Rotationsverdampfen des THF wird im Vakuum bei 70°C getrocknet.
Ausbeute: 2,69 g (89,7 % der Theorie) Fp. 62°C
In entsprechender Weise wurden Verbindungen der Formel (Id) hergestellt:
Zwischenprodukte
Beispiel 5'
Zu 182 ml (1,157 Mol) Pipecolinsäureethylester und 162 ml (1,157 Mol) Triethylamin in 1.200 ml absolutem Tetrahydrofuran (THF) tropft man bei 0 bis 10°C 223 g (1,125 Mol) Mesitylenessigsäurechlorid und rührt 1 Stunde bei Raumtemperatur nach. Nach Einrühren in 5 l Eiswasser und 500 ml 1 N HCl wird das Produkt abgesaugt, mit Wasser nachgewaschen und bei 50°C im Vakuum über P2O5 getrocknet. Man erhält 342,3 g (95,2 % der Theorie) N-(2,4,6-Trimethylphenylacetyl)-piperidin-2-carbonsäureethylester.
Beispiel 37'
Zu 115 g (1 Mol) L-Prolin in 1 l Wasser gibt man 20 g (0,5 Mol) NaOH-Plätzchen. Bei einer Temperatur unter 40°C werden synchron 60 g (1,5 Mol) NaOH in 300 ml Wasser und 197,6 g (1 Mol) Mesitylenessigsäurechlorid zugetropft und 1 Stunde nachgerührt. Anschließend wird bei 5 bis 20°C mit konzentrierter Salzsäure angesäuert, das Produkt abgesaugt und im Vakuum bei 70°C über P2O5 getrocknet.
Ausbeute: 262 g (95,3 % der Theorie) N-2,4,6-Trimethylphenylacetylprolin Fp. 156°C
Beispiel 26'
137,5 g (0,5 Mol) N-2,4,6-Trimethylphenylacetyl-prolin werden in 500 ml Methanol gelöst. Nach Zugabe von 73 ml (0,55 Mol) Dimethoxypropan und 4,75 g (25 mMol) p-Toluolsulfonsäure-monohydrat erhitzt man 2 Stunden unter Rückfluß. Nach Einrotieren wird der Rückstand in Methylenchlorid aufgenommen, mit Natriumhydrogencarbonat-Lösung gewaschen, die Methylenchlorid-Phase getrocknet und einrotiert. Nach Umkristallisieren aus Methylenchlorid/Methyl-tert.-butylether/n-Hexan wurden 107,9 g (74,7 %) N-(2,4,6-Trimethylphenylacetyl)-pyrrolidin-2-carbonsäuremethylester erhalten. Fp. 74°C.
Die Wirkstoffe eignen sich zur Bekämpfung von tierischen Schädlingen, vorzugsweise Arthropoden und Nematoden, insbesondere Insekten und Spinnentieren, die in der Landwirtschaft, in Forsten, im Vorrats- und Materialschutz sowie auf dem Hygienesektor vorkommen. Sie sind gegen normal sensible und resistente Arten sowie gegen alle oder einzelne Entwicklungsstadien wirksam. Zu den oben erwähnten Schädlingen gehören:
Aus der Ordnung der Isopoda z.B. Oniscus asellus, Armadillidium vulgare, Porcellio scaber.
Aus der Ordnung der Diplopoda z.B. Blaniulus guttulatus.
Aus der Ordnung der Chilopoda z.B. Geophilus carpophagus, Scutigera spec.
Aus der Ordnung der Symphyla z.B. Scutigerella immaculata.
Aus der Ordnung der Thysanura z.B. Lepisma saccharina.
Aus der Ordnung der Collembola z.B. Onychiurus armatus.
Aus der Ordnung der Orthoptera z.B. Blatta orientalis, Periplaneta americana, Leucophaea maderae, Blattella germanica, Acheta domesticus, Gryllotalpa spp., Locusta migratoria migratorioides, Melanoplus differentialis, Schistocerca gregaria.
Aus der Ordnung der Dermaptera z.B. Forficula auricularia.
Aus der Ordnung der Isoptera z.B. Reticulitermes spp..
Aus der Ordnung der Anoplura z.B. Phylloxera vastatrix, Pemphigus spp., Pediculus humanus corporis, Haematopinus spp., Linognathus spp.
Aus der Ordnung der Mallophaga z.B. Trichodectes spp., Damalinea spp.
Aus der Ordnung der Thysanoptera z.B. Hercinothrips femoralis, Thrips tabaci.
Aus der Ordnung der Heteroptera z.B. Eurygaster spp., Dysdercus intermedius, Piesma quadrata, Cimex lectularius, Rhodnius prolixus, Triatoma spp.
Aus der Ordnung der Homoptera z.B. Aleurodes brassicae, Bemisia tabaci, Trialeurodes vaporariorum, Aphis gossypii, Brevicoryne brassicae, Cryptomyzus ribis, Aphis fabae, Doralis pomi, Eriosoma lanigerum, Hyalopterus arundinis, Macrosiphum avenae, Myzus spp., Phorodon humuli, Rhopalosiphum padi, Empoasca spp., Euscelis bilobatus, Nephotettix cincticeps, Lecanium corni, Saissetia oleae, Laodelphax striatellus, Nilaparvata lugens, Aonidiella aurantii, Aspidiotus hederae, Pseudococcus spp. Psylla spp.
Aus der Ordnung der Lepidoptera z.B. Pectinophora gossypiella, Bupalus piniarius, Cheimatobia brumata, Lithocolletis blancardella, Hyponomeuta padella, Plutella maculipennis, Malacosoma neustria, Euproctis chrysorrhoea, Lymantria spp. Bucculatrix thurberiella, Phyllocnistis citrella, Agrotis spp., Euxoa spp., Feltia spp., Earias insulana, Heliothis spp., Spodoptera exigua, Mamestra brassicae, Panolis flammea, Prodenia litura, Spodoptera spp., Trichoplusia ni, Carpocapsa pomonella, Pieris spp., Chilo spp., Pyrausta nubilalis, Ephestia kuehniella, Galleria mellonella, Tineola bisselliella, Tinea pellionella, Hofmannophila pseudospretella, Cacoecia podana, Capua reticulana, Choristoneura fumiferana, Clysia ambiguella, Homona magnanima, Tortrix viridana.
Aus der Ordnung der Coleoptera z.B. Anobium punctatum, Rhizopertha dominica, Acanthoscelides obtectus, Acanthoscelides obtectus, Hylotrupes bajulus, Agelastica alni, Leptinotarsa decemlineata, Phaedon cochleariae, Diabrotica spp., Psylliodes chrysocephala, Epilachna varivestis, Atomaria spp., Oryzaephilus surinamensis, Anthonomus spp., Sitophilus spp., Otiorrhynchus sulcatus, Cosmopolites sordidus, Ceuthorrhynchus assimilis, Hypera postica, Dermestes spp., Trogoderma spp., Anthrenus spp., Attagenus spp., Lyctus spp., Meligethes aeneus, Ptinus spp., Niptus hololeucus, Gibbium psylloides, Tribolium spp., Tenebrio molitor, Agriotes spp., Conoderus spp., Melolontha melolontha, Amphimallon solstitialis, Costelytra zealandica.
Aus der Ordnung der Hymenoptera z.B. Diprion spp., Hoplocampa spp., Lasius spp., Monomorium pharaonis, Vespa spp.
Aus der Ordnung der Diptera z.B. Aedes spp., Anopheles spp., Culex spp., Drosophila melanogaster, Musca spp., Fannia spp., Calliphora erythrocephala, Lucilia spp., Chrysomyia spp., Cuterebra spp., Gastrophilus spp., Hyppobosca spp., Stomoxys spp., Oestrus spp., Hypoderma spp., Tabanus spp., Tannia spp., Bibio hortulanus, Oscinella frit, Phorbia spp., Pegomyia hyoscyami, Ceratitis capitata, Dacus oleae, Tipula paludosa.
Aus der Ordnung der Siphonaptera z.B. Xenopsylla cheopis, Ceratophyllus spp..
Aus der Ordnung der Arachnida z.B. Scorpio maurus, Latrodectus mactans.
Aus der Ordnung der Acarina z.B. Acarus siro, Argas spp., Ornithodorus spp., Dermanyssus gallinae, Eriophyes ribis, Phyllocoptruta oleivora, Boophilus spp., Rhipicephalus spp., Amblyomma spp., Hyalomma spp., Ixodes spp., Psoroptes spp., Chorioptes spp., Sarcoptes spp., Tarsonemus spp., Bryobia praetiosa, Panonychus spp., Tetranychus spp..
Zu den pflanzenparasitären Nematoden gehören Pratylenchus spp., Radopholus similis, Ditylenchus dipsaci, Tylenchulus semipenetrans, Heterodera spp., Meloidogyne spp., Aphelenchoides spp., Longidorus spp., Xiphinema spp., Trichodorus spp..
Die erfindungsgemäßen Wirkstoffe können weiterhin als Defoliants, Desiccants, Krautabtötungsmittel und insbesondere als Unkrautvernichtungsmittel verwendet werden. Unter Unkraut im weitesten Sinne sind alle Pflanzen zu verstehen, die an Orten aufwachsen, wo sie unerwünscht sind. Ob die erfindungsgemäßen Stoffe als totale oder selektive Herbizide wirken, hängt im wesentlichen von der angewendeten Menge ab.
Charakteristisch für die erfindungsgemäßen Verbindungen ist, daß sie eine selektive Wirksamkeit gegen monokotyle Unkräuter im Vor- und Nachlaufverfahren (Pre- und Postemergence) bei guter Kulturflanzenverträglichkeit aufweisen.
Die erfindungsgemäßen Wirkstoffe können z.B. bei den folgenden Pflanzen verwendet werden:
Monokotyle Unkräuter der Gattungen: Echinochloa, Setaria, Panicum, Digitaria, Phleum, Poa, Festuca, Eleusine, Brachiaria, Lolium, Bromus, Avena, Cyperus, Sorghum, Agropyron, Cynodon, Monochoria, Fimbristylis, Sagittaria, Eleocharis, Scirpus, Paspalum, Ischaemum, Sphenoclea, Dactyloctenium, Agrostis, Alopecurus, Apera.
Monokotyle Kulturen der Gattungen: Oryza, Zea, Triticum, Hordeum, Avena, Secale, Sorghum, Panicum, Saccharum, Ananas, Asparagus, Allium.
Die Verwendung der erfindungsgemäßen Wirkstoffe ist jedoch keineswegs auf diese Gattungen beschränkt, sondern erstreckt sich in gleicher Weise auch auf andere Pflanzen.
Die Verbindungen eignen sich in Abhängigkeit von der Konzentration zur Totalunkrautbekämpfung z.B. auf Industrie- und Gleisanlagen und auf Wegen und Plätzen mit und ohne Baumbewuchs. Ebenso können die Verbindungen zur Unkrautbekämpfung in Dauerkulturen, z.B. Forst, Ziergehölz-, Obst-, Wein-, Citrus-, Nuß-, Bananen-, Kaffee-, Tee-, Gummi-, Ölpalm-, Kakao-, Beerenfrucht- und Hopfenanlagen und zur selektiven Unkrautbekämpfung in einjährigen Kulturen eingesetzt werden.
Dabei zeigen die erfindungsgemäßen Wirkstoffe neben einer hervorragenden Wirkung gegen Schadpflanzen gute Verträglichkeit gegenüber wichtigen Kulturpflanzen, wie z. B. Weizen, Baumwolle, Sojabohnen, Citrusfrüchten und Zuckerrüben, und können daher als selektive Unkrautbekämpfungsmittel eingesetzt werden.
Die Wirkstoffe können in die üblichen Formulierungen übergeführt werden, wie Lösungen, Emulsionen, Suspensionen, Pulver, Schäume, Pasten, Granulate, Aerosole, Wirkstoff-imprägnierte Natur- und synthetische Stoffe, Feinstverkapselungen in polymeren Stoffen und in Hüllmassen für Saatgut, ferner in Formulierungen mit Brennsätzen, wie Räucherpatronen, -dosen, -spiralen u.ä., sowie ULV-Kalt- und Warmnebel-Formulierungen.
Diese Formulierungen werden in bekannter Weise hergestellt, z.B. durch Vermischen der Wirkstoffe mit Streckmitteln, also flüssigen Lösungsmitteln, unter Druck stehenden verflüssigten Gasen und/oder festen Trägerstoffen, gegebenenfalls unter Verwendung von oberflächenaktiven Mitteln, also Emulgiermitteln und/oder Dispergiermitteln und/oder schaumerzeugenden Mitteln. Im Falle der Benutzung von Wasser als Streckmittel können z.B. auch organische Lösungsmittel als Hilfslösungsmittel verwendet werden. Als flüssige Lösungsmittel kommen im wesentlichen in Frage: Aromaten, wie Xylol, Toluol, oder Alkylnaphthaline, chlorierte Aromaten oder chlorierte aliphatische Kohlenwasserstoffe, wie Chlorbenzole, Chlorethylene oder Methylenchlorid, aliphatische Kohlenwasserstoffe, wie Cyclohexan oder Paraffine, z.B. Erdölfraktionen, Alkohole, wie Butanol oder Glycol sowie deren Ether und Ester, Ketone, wie Aceton, Methylethylketon, Methylisobutylketon oder Cyclohexanon, stark polare Lösungsmittel, wie Dimethylformamid und Dimethylsulfoxid, sowie Wasser; mit verflüssigten gasförmigen Streckmitteln oder Trägerstoffen sind solche Flüssigkeiten gemeint, welche bei normaler Temperatur und unter Normaldruck gasförmig sind, z.B. Aerosol-Treibgas, wie Halogenkohlenwasserstoffe sowie Butan, Propan, Stickstoff und Kohlendioxid; als feste Trägerstoffe kommen in Frage: z.B. natürliche Gesteinsmehle, wie Kaoline, Tonerden, Talkum, Kreide, Quarz, Attapulgit, Montmorillonit oder Diatomeenerde und synthetische Gesteinsmehle, wie hochdisperse Kieselsäure, Aluminiumoxid und Silikate; als feste Trägerstoffe für Granulate kommen in Frage: z.B. gebrochene und fraktionierte natürliche Gesteine wie Calcit, Marmor, Bims, Sepiolith, Dolomit sowie synthetische Granulate aus anorganischen und organischen Mehlen sowie Granulate aus organischem Material wie Sägemehl, Kokosnußschalen, Maiskolben und Tabakstengel; als Emulgier und/oder schaumerzeugende Mittel kommen in Frage: z.B. nichtionogene und anionische Emulgatoren, wie Polyoxyethylen-Fettsäure-Ester, Polyoxyethylen-Fettalkohol-Ether, z.B. Alkylarylpolyglykol-Ether, Alkylsulfonate, Alkylsulfate, Arylsulfonate sowie Eiweißhydrolysate; als Dispergiermittel kommen in Frage: z.B. Lignin-Sulfitablaugen und Methylcellulose.
Es können in den Formulierungen Haftmittel wie Carboxymethylcellulose, natürliche und synthetische pulverige, körnige oder latexförmige Polymere verwendet werden, wie Gummiarabicum, Polyvinylalkohol, Polyvinylacetat, sowie natürliche Phospholipide, wie Kephaline und Lecithine, und synthetische Phospholipide. Weitere Additive können mineralische und vegetabile Öle sein.
Es können Farbstoffe wie anorganische Pigmente, z.B. Eisenoxid, Titanoxid, Ferrocyanblau und organische Farbstoffe, wie Alizarin-, Azo- und Metallphthalocyaninfarbstoffe und Spurennährstoffe wie Salze von Eisen, Mangan, Bor, Kupfer, Kobalt, Molybdän und Zink verwendet werden. Die Formulierungen enthalten im allgemeinen zwischen 0,1 und 95 Gewichtsprozent Wirkstoff, vorzugsweise zwischen 0,5 und 90 %.
Die erfindungsgemäßen Wirkstoffe können in ihren handelsüblichen Formulierungen sowie in den aus diesen Formulierungen bereiteten Anwendungsformen in Mischung mit anderen Wirkstoffen, wie Insektiziden, Lockstoffen, Sterilantien, Akariziden, Nematiziden Herbiziden oder Fungiziden vorliegen. Zu den Insektiziden zählen beispielsweise Phosphorsäureester, Carbamate, Carbonsäureester, chlorierte Kohlenwasserstoffe, Phenylharnstoffe, durch Mikroorganismen hergestellte Stoffe u.a.
Die erfindungsgemäßen Wirkstoffe können ferner in ihren handelsüblichen Formulierungen sowie in den aus diesen Formulierungen bereiteten Anwendungsformen in Mischung mit Synergisten vorliegen. Synergisten sind Verbindungen, durch die die Wirkung der Wirkstoffe gesteigert wird, ohne daß der zugesetzte Synergist selbst aktiv wirksam sein muß.
Der Wirkstoffgehalt der aus den handelsüblichen Formulierungen bereiteten Anwendungsformen kann in weiten Bereichen variieren. Die Wirkstoffkonzentration der Anwendungsformen kann von 0,0000001 bis zu 95 Gew.-% Wirkstoff, vorzugsweise zwischen 0,0001 und 1 Gew.-% liegen.
Die Anwendung geschieht in einer den Anwendungsformen angepaßten üblichen Weise.
Die erfindungsgemäß verwendbaren Wirkstoffe eignen sich auch zur Bekämpfung von Milben, Zecken usw. auf dem Gebiet der Tierhaltung und Viehzucht, wobei durch die Bekämpfung der Schädlinge bessere Ergebnisse, z.B. höhere Milchleistungen, höheres Gewicht, schöneres Tierfell, längere Lebensdauer usw. erreicht werden können.
Die Anwendung der erfindungsgemäß verwendbaren Wirkstoffe geschieht auf diesem Gebiet in bekannter Weise wie durch orale Anwendung in Form von beispielsweise Tabletten, Kapseln, Tränken, Granulaten, durch dermale bzw. äußerliche Anwendung in Form beispielsweise des Tauchens (Dippen), Sprühens (Sprayen), Aufgießens (pour-on and spot-on) und des Einpuderns sowie durch parenterale Anwendung in Form beispielsweise der Injektion sowie ferner durch das "feed-through"-Verfahren. Daneben ist auch eine Anwendung als Formkörper (Halsband, Ohrmarke) möglich.
Die erfindungsgemäßen Verbindungen der Formel (I) weisen antimikrobielle, insbesondere starke antibakterielle und antimykotische Wirkungen auf. Sie besitzen ein sehr breites antimykotisches Wirkungsspektrum, insbesondere gegen Dermatophyten und Sproßpilze sowie biphasische Pilze, z.B. gegen Candida-Arten wie Candida albicans, Epidermophyton-Arten wie Epidermophyton floccosum, Aspergillus-Arten wie Aspergillus niger und Aspergillus fumigatus, Trichophyton-Arten wie Trichophyton mentagrophytes, Microsporon-Arten wie Microsporon felineum sowie Torulopsis-Arten wie Torulopsis glabrata. Die Aufzählung dieser Mikroorganismen stellt keinesfalls eine Beschränkung der bekämpfbaren Keime dar, sondern hat nur erläuternden Charakter.
Als Indikationsbeispiele in der Humanmedizin können beispielsweise genannt werden:
Dermatomykosen und Systemmykosen durch Trichophyton mentagrophytes und andere Trichophytonarten, Microsporonarten sowie Epidermophyton floccosum, Sproßpilze und biphasische Pilze sowie Schimmelpilze hervorgerufen.
Als Indikationsgebiet in der Tiermedizin können beispielsweise aufgeführt werden:
Alle Dermatomykosen und Systemmykosen, insbesondere solche, die durch die obengenannten Erreger hervorgerufen werden.
Zur vorliegenden Erfindung gehören pharmazeutische Zubereitungen, die neben nicht toxischen, inerten pharmazeutisch geeigneten Trägerstoffen einen oder mehrere erfindungsgemäße Wirkstoffe enthalten oder die aus einem oder mehreren erfindungsgemäßen Wirkstoffen bestehen.
Zur vorliegenden Erfindung gehören auch pharmazeutische Zubereitungen in Dosierungseinheiten. Dies bedeutet, daß die Zubereitungen in Form einzelner Teile, z.B. Tabletten, Dragees, Kapseln, Pillen, Suppositorien und Ampullenvorliegen, deren Wirkstoffgehalt einen Bruchteil oder einem Vielfachen einer Einzeldosis entspricht. Die Dosierungseinheiten können z.B. 1,2,3 oder 4 Einzeldosen oder 1/2, 1/3 oder 1/4 einer Einzeldosis enthalten. Eine Einzeldosis enthält vorzugsweise die Menge Wirkstoff, die bei einer Applikation verabreicht wird und die gewöhnlich einer ganzen, einer halben oder einem Drittel oder einem Viertel einer Tagesdosis entspricht.
Unter nicht toxischen, inerten pharmazeutisch geeigneten Trägerstoffen sind feste, halbfeste oder flüssige Verdünnungsmittel, Füllstoffe oder Formulierungshilfsmittel jeder Art zu verstehen.
Als bevorzugte pharmazeutische Zubereitungen seien Tabletten, Dragees, Kapseln, Pillen, Granulate, Suppositorien, Lösungen, Suspensionen und Emulsionen, Pasten, Salben, Gele, Cremes, Lotions, Puder oder Sprays genannt.
Tabletten, Dragees, Kapseln, Pillen und Granulate können den oder die Wirkstoffe neben den üblichen Trägerstoffen enthalten, wie (a) Füll- und Streckmittel, z.B. Stärken, Milchzucker, Rohrzucker, Glucose, Mannit und Kieselsäure re, (b) Bindemittel, z.B. Carboxymethylcellulose, Alginate, Gelantine, Polyvinylpyrrolidon, (c) Feuchthaltemittel, z.B. Glycerin, (d) Sprengmittel, z.B. Agar-Agar, Calciumcarbonat und Natriumcarbonat, (e) Lösungsverzögerer, z.B. Paraffin und (f) Resorptionsbeschleuniger, z.B. quarternäre Ammoniumverbindungen, (g) Netzmittel, z.B. Cetylalkohol, Glycerinmonostearat, (h) Adsorptionsmittel, z.B. Kaolin und Bentonit und (i) Gleitmittel, z.B. Talkum, Calcium- und Magnesiumstearat und feste Polyethylenglykole oder Gemische der unter (a) bis (i) aufgeführten Stoffe.
Die Tabletten, Dragees, Kapseln, Pillen und Granulate können mit den üblichen gegebenenfalls Opakisierungsmittel enthaltenden Überzügen und Hüllen versehen sein und so zusammengesetzt sein, daß sie den oder die Wirkstoffe nur oder bevorzugt in einem bestimmten Teil des Intestinaltraktes, gegebenenfalls verzögert abgeben, wobei als Einbettungsmassen, z.B. Polymersubstanzen und Wachse verwendet werden können.
Der oder die Wirkstoffe können gegebenenfalls mit einem oder mehreren der oben angegebenen Trägerstoffe auch in mikroverkapselter Form vorliegen.
Suppositorien können neben dem oder den Wirkstoffen die üblichen wasserlöslichen oder wasserunlöslichen Trägerstoffe enthalten, z.B. Polyethylenglykole, Fette, z.B. Kakaofett und höhere Ester (z.B. C14-Alkohol mit C16-Fettsäure) oder Gemische dieser Stoffe.
Salben, Pasten, Cremes und Gele können neben dem oder den Wirkstoffen die üblichen Trägerstoffe enthalten, z.B. tierische und pflanzliche Fette, Wachse, Paraffine, Stärke, Tragant, Cellulosederivate, Polyethylenglykole, Silicone, Bentonite, Kieselsäure, Talkum und Zinkoxid oder Gemische dieser Stoffe.
Puder und Sprays können neben dem oder den Wirkstoffen die üblichen Trägerstoffe enthalten, z.B. Milchzucker, Talkum, Kieselsäure, Aluminiumhydroxid, Calciumsilikat und Polyamidpulver oder Gemische dieser Stoffe, Sprays können zusätzlich die üblichen Treibmittel z.B. Chlorfluorkohlenwasserstoffe enthalten.
Lösungen und Emulsionen können neben dem oder den Wirkstoffen die üblichen Trägerstoffe wie Lösungsmittel, Lösungsverzögerer und Emulgatoren, z.B. Wasser, Ethylalkohol, Isopropylalkohol, Ethylcarbonat,Ethylacetat, Benzylalkohol, Benzylbenzoat, Propylenglykol, 1,3-Buty lenglykol, Dimethylformamid, Öle, insbesondere Baumwollsaatöl, Erdnußöl, Maiskeimöl, Olivenöl, Ricinusöl und Sesamöl, Glycerin, Glycerinformal, Tetrahydrofurfurylalkohol, Polyethylenglykole und Fettsäureester des Sorbitans oder Gemische dieser Stoffe enthalten.
Zur parenteralen Applikation können die Lösungen und Emulsionen auch in steriler und blutisotonischer Form vorliegen.
Suspensionen können neben dem oder den Wirkstoffen die üblichen Trägerstoffe, wie flüssige Verdünnungsmittel, z.B. Wasser, Ethylalkohol, Propylalkohol, Suspendiermittel, z.B. ethoxylierte Isostearylalkohole, Polyoxyethylensorbit- und -sorbitanester, mikrokristalline Cellulose, Aluminiummetahydroxid, Bentonit, Agar-Agar und Tragant oder Gemische dieser Stoffe enthalten.
Die genannten Formulierungsformen können auch Färbemittel, Konservierungsstoffe sowie geruchs- und geschmacksverbessernde Zusätze, z.B. Pfefferminzöl und Eukalyptusöl und Süßmittel, z.B. Saccarin enthalten.
Die therapeutisch wirksamen Verbindungen sollen in den oben angeführten pharmazeutischen Zubereitungen vorzugsweise in einer Konzentration von etwa 0,1 bis 99,5, vorzugsweise von 0,5 bis 95 Gew.-% der Gesamtmischung vorhanden sein.
Die oben aufgeführten pharmazeutischen Zubereitungen können außer den erfindungsgemäßen Wirkstoffen auch weitere pharmazeutische Wirkstoffe enthalten.
Die Herstellung der oben aufgeführten pharmazeutischen Zubereitungen erfolgt in üblicher Weise nach bekannten Methoden, z.B. durch Mischen des oder der Wirkstoffe mit dem oder den Trägerstoffen.
Zur vorliegenden Erfindung gehört auch die Verwendung der erfindungsgemäßen Wirkstoffe, sowie von pharmazeutischen Zubereitungen, die einen oder mehrere erfindungsgemäße Wirkstoffe enthalten, in der Human- und Veterinärmedizin zur Verhütung, Besserung und/oder Heilung der oben aufgeführten Erkrankungen.
Die Wirkstoffe oder die pharmazeutischen Zubereitungen können lokal, oral, parenteral, intraperitoneal und/oder rektal, vorzugsweise parenteral, insbesondere intravenös appliziert werden.
Im allgemeinen hat es sich sowohl in der Human- als auch in der Veterinärmedizin als vorteilhaft erwiesen, den oder die erfindungsgemäßen Wirkstoffe in Gesamtmengen von etwa 2,5 bis etwa 200, vorzugweise von 5 bis 150 mg/kg Körpergewicht je 24 Stunden, gegebenenfalls in Form mehrerer Einzelgaben zur Erzielung der gewünschten Ergebnisse zu verabreichen.
Bei oralen Applikationen werden die erfindungsgemäßen Wirkstoffe in Gesamtmengen von etwa 2,5 bis etwa 200, vorzugsweise von 5 bis 150 mg/kg Körpergewicht je 24 Stunden und bei parenteraler Applikation in Gesamtmengen von etwa 2,5 bis etwa 50, vorzugsweise von 1 bis 25 mg/kg Körpergewicht je 24 Stunden verabreicht.
Es kann jedoch erforderlich sein, von den genannten Dosierungen abzuweichenund zwar in Abhängigkeit von der Art und dem Körpergewicht des zu behandelnden Objektes, der Art und Schwere der Erkrankung, der Art der Zubereitung und der Applikation des Arzneimittels sowie dem Zeitraum bzw. Intervall, innerhalb welchem die Verabreichung erfolgt. So kann es in einigen Fällen ausreichend sein, mit weniger als der obengenannten Menge Wirkstoff auszukommen, während in anderen Fällen die oben angeführte Wirkstoffmenge überschritten werden muß. Die Festlegung der jeweils erforderlichen optimalen Dosierung und Applikationsart der Wirkstoffe kann durch jeden Fachmann aufgrund seines Fachwissens leicht erfolgen.
Beispiel A
Tetranychus-Test (resistent)
Lösungsmittel: 7 Gewichtsteile Dimethylformamid Emulgator: 1 Gewichtsteil Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel und der angegebenen Menge Emulgator und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Bohnenpflanzen (Phaseolus vulgaris), die stark von allen Entwicklungsstadien der gemeinen Spinnmilbe oder Bohnenspinnmilbe (Tetranychus urticae) befallen sind, werden durch Tauchen in die Wirkstoffzubereitung der gewünschten Konzentration behandelt.
Nach der gewünschten Zeit wird die Abtötung in % bestimmt. Dabei bedeutet 100 %, daß alle Spinnmilben abgetötet wurden; 0 % bedeutet, daß keine Spinnmilben abgetötet wurden.
Bei diesem Test zeigen z.B. die folgenden Verbindungen der Herstellungsbeispiele überlegene Wirksamkeit gegenüber dem Stand der Technik (88).
Beispiel B
Pre-emergence-Test
Lösungsmittel: 5 Gewichtsteile Aceton Emulgator: 1 Gewichtsteil Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel, gibt die angegebene Menge Emulgator zu und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Samen der Testpflanzen werden in normalen Boden ausgesät und nach 24 Stunden mit der Wirkstoffzubereitung begossen. Dabei hält man die Wassermenge pro Flächeneinheit zweckmäßigerweise konstant. Die Wirkstoffkonzentration in der Zubereitung spielt keine Rolle, entscheidend ist nur die Aufwandmenge des Wirkstoffs pro Flächeneinheit. Nach drei Wochen wird der Schädigungsgrad der Pflanzen bonitiert in % Schädigung im Vergleich zur Entwicklung der unbehandelten Kontrolle. Es bedeuten:
&numsp &numsp 0 % = keine Wirkung (wie unbehandelte Kontrolle)
100 % = totale Vernichtung
Bei diesem Test zeigen zeigen z.B. die folgenden Verbindungen der Herstellungsbeispiele überlegene Wirksamkeit gegenüber dem Stand der Technik: (1), (13).
Beispiel C
Post-emergence-Test
Lösungsmittel: 5 Gewichtsteile Aceton Emulgator: 1 Gewichtsteil Alkylarylpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man 1 Gewichtsteil Wirkstoff mit der angegebenen Menge Lösungsmittel, gibt die angegebene Menge Emulgator zu und verdünnt das Konzentrat mit Wasser auf die gewünschte Konzentration.
Mit der Wirkstoffzubereitung spritzt man Testpflanzen, welche eine Höhe von 5 - 15 cm haben so, daß die jeweils gewünschten Wirkstoffmengen pro Flächeneinheit ausgebracht werden. Die Konzentration der Spritzbrühe wird so gewählt, daß in 2000 l Wasser/ha die jeweils gewünschten Wirkstoffmengen ausgebracht werden. Nach drei Wochen wird der Schädigungsgrad der Pflanzen bonitiert in % Schädigung im Vergleich zur Entwicklung der unbehandelten Kontrolle.
&numsp &numsp 0 % = keine Wirkung (wie unbehandelte Kontrolle)
100 % = totale Vernichtung
Bei diesem Test zeigen z.B. die folgenden Verbindungen der Herstellungsbeispiele überlegene Wirksamkeit gegenüber dem Stand der Technik: (1), (13).
Beispiel D
Test mit Lucilia cuprina resistent-Larven
Emulgator: 35 Gewichtsteile Ethylenglykolmonomethylether
35 Gewichtsteile Nonylphenolpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man drei Gewichtsteile Wirkstoff mit sieben Gewichtsteilen des oben angegebenen Gemisches und verdünnt das so erhaltene Konzentrat mit Wasser auf die jeweils gewünschte Konzentration.
Etwa 20 Lucilia cuprina res.-Larven werden in ein Teströhrchen gebracht, welches ca. 1 cm 3 Pferdefleisch und 0,5 ml der Wirkstoffzubereitung enthält. Nach 24 Stunden wird der Abtötungsgrad bestimmt.
Bei diesem Test zeigen z.B. die folgenden Verbindungen der Herstellungsbeispiele eine stark ausgeprägte Wirksamkeit: 7, 54, 58, 62, 64, 67, 68, 213, 215, 216, 217, 222.
Beispiel E
Test mit Psoroptes ovis
Emulgator: 35 Gewichtsteile Ethylenglykolmonomethylether
35 Gewichtsteile Nonylphenolpolyglykolether
Zur Herstellung einer zweckmäßigen Wirkstoffzubereitung vermischt man drei Gewichtsteile Wirkstoff mit sieben Gewichtsteilen des oben angegebenen Gemisches und verdünnt das so erhaltene Konzentrat mit Wasser auf die gewünschte Konzentration.
Etwa 10 - 25 Psoroptes ovis werden in 1 ml der zu testenden Wirkstoffzubereitung gebracht, die in Tablettennester einer Tiefziehverpackung pipettiert wurden. Nach 24 Stunden wird der Abtötungsgrad bestimmt.
Bie diesem Test zeigen z.B. die folgenden Verbindungen der Herstellungsbeispiele eine stark ausgeprägte Wirksamkeit: 39, 55, 57, 62, 87, 89, 167, 201, 245.
Beispiel F
Antimykotische in-vitro-Wirksamkeit
Versuchsbeschreibung:
Die in-vitro-Prüfungen wurden mit Keiminokula von durchschnittlich 1 x 10 4 Keimen/ml Substrat durchgeführt. Als Nährmedium diente Yeast Nitrogen Base-Medium für Hefen und Kimmig-Medium für Schimmelpilze und Dermatophyten.
Die Bebrütungstemperatur betrug 37 °C bei Hefen und 28 °C bei Schimmelpilzen und Dermatophyten, die Bebrütungsdauer lag bei 24 bis 96 Stunden bei Hefen und 96 bis 120 Stunden bei Dermatophyten und Schimmelpilzen.
Die Beurteilung der Fungizide erfolgt durch Ausplattieren und erneutes Bebrüten voll gehemmter Ansätze, wobei fungizide Konzentrationen weniger als 100 Keime c.f.n. (colony forming unit) pro ml enthalten.
In diesem Test zeigen die erfindungsgemäßen Verbindungen der Formel (I) gemäß den Herstellungsbeispielen 36, 40, 85, 91, 114, 116, 120, 167, 170, 174, 176, 178, 182, 184, 188, 194 eine stark ausgeprägte antimykotische Wirksamkeit.









































Комментариев нет:
Отправить комментарий